Похожие презентации:
Формування поняття про окисно-відновні реакції в процес і вивчення шкільного курсу хімії
1.
Ковальчук Олег РомановичвФОРМУВАННЯ ПОНЯТТЯ ПРО ОКИСНО-ВІДНОВНІ
РЕАКЦІЇ В ПРОЦЕС І ВИВЧЕННЯ ШКІЛЬНОГО
КУРСУ ХІМІЇ
Магістерська робота
Наук. керівник:
доц. Гладюк М.М.
2023 рік
1
2.
• Актуальність теми магістерської роботи:Необхідність переосмислення методичних підходів
до формування загальнохімічного поняття про
хімічну реакцію та окисно-відновні процеси
зокрема в шкільному курсі хімії зумовлюють.
• Предметом дослідження стали дидактичні
завдання для формування в учнів знань про хімічну
реакцію в цілому та окисно-відновні процеси
зокрема, та методика їх використання у 8-9 класах.
• Мета роботи полягає у розробці та апробації
комплексу дидактичних завдань для формування в
учнів знань про хімічну реакцію у 8-9 класах.
2
3.
Завдання дослідження:• На основі аналізу навчально-методичної літератури
виявити основні підходи до визначення поняття
„формування знань про хімічну реакцію”.
• З’ясувати місце спеціально сконструйованих
дидактичних завдань в загальній системі навчання
хімії.
• Розробити комплекс дидактичних завдань для
формування в учнів знань про окисно-відновні
процеси у 8-9 класах.
• Апробувати розроблену систему завдань в умовах
реального навчально-виховного процесу.
3
4.
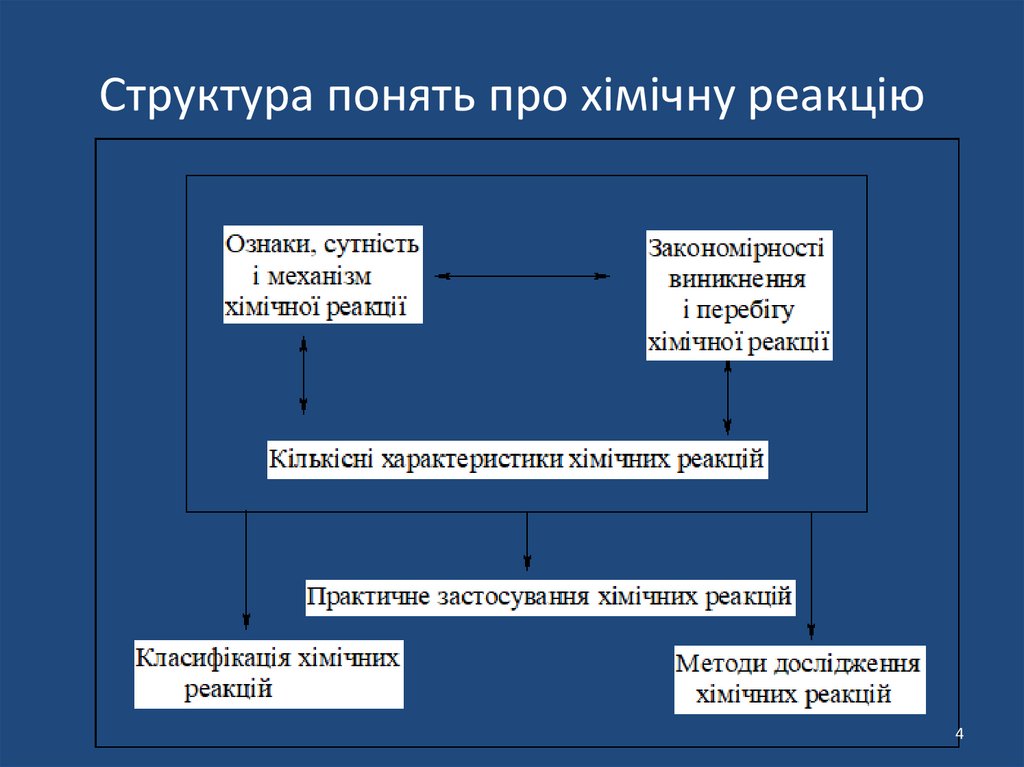
Структура понять про хімічну реакцію4
5.
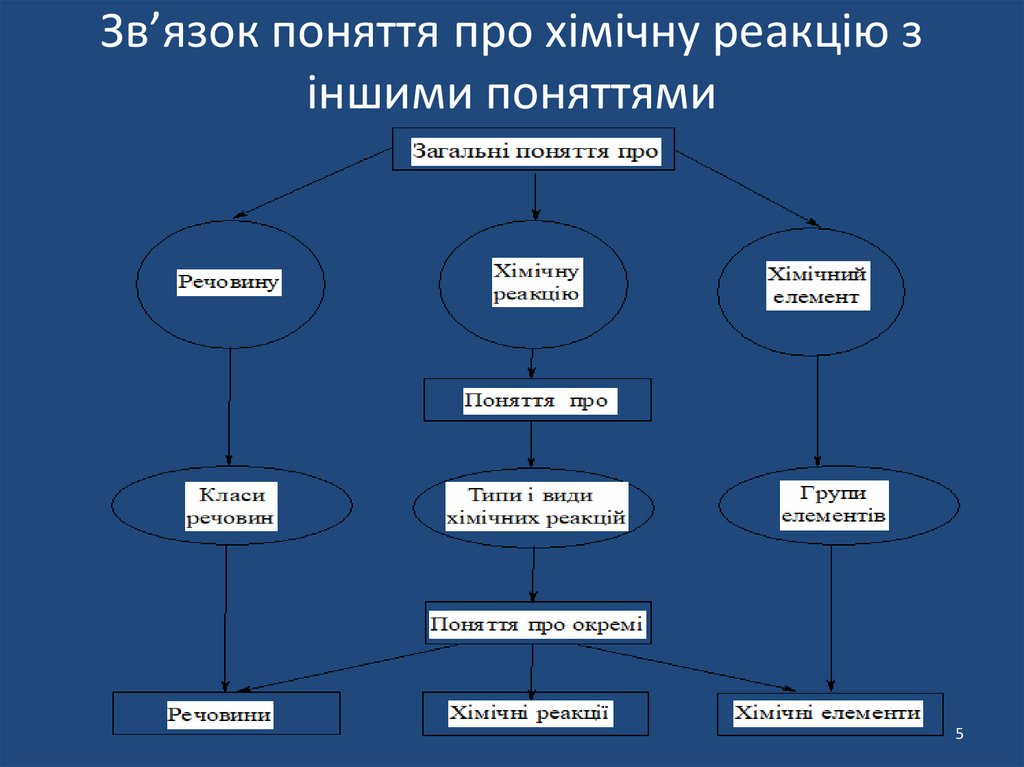
Зв’язок поняття про хімічну реакцію зіншими поняттями
5
6.
Завдання для організації пізнавальної діяльності учнів в процесізасвоєння понять „Ступінь окиснення. Окисно-відновні реакції”
Завдання 1. З переліку речовин випишіть ті, в яких атоми мають
ступінь окиснення „0”: NаСl; Н2; КМnО4; С; НСl; Ва; Аl2О3; О2; Сl2; Fе(ОН)2.
Завдання 2. Визначте ступінь окиснення кожного хімічного елемента в
таких сполуках: КСl; КСlО3; МgСl2; Сl2; КМnО4; К2МnО4; Н3РО4.
Завдання
3.
Визначте
ступінь
окиснення
Сульфуру
в
кристалах
речовин, молекулах та йонах: Аl2(SО4)3; Nа2SО4; Н2S; SО2; SО 24 ; НSО 4 .
Завдання 4. Визначте валентність і ступінь окиснення Карбону за
структурними формулами речовин:
H
H
C
H
H
H
H
C
H
O
H
H
C
O
O
H
H
C
O
H
Завдання 6. Визначте ступінь окиснення Мангану і сполуках: КМnО4;
МnО2; Мn2О7; Мn; К2МnО4; МnО. Випишіть формули речовин, які є: а) лише
окисниками; б) лише відновниками; в) тих, що можуть бути і окисниками, і
відновниками.
Завдання 7. Використовуючи дані про розподіл електронів в атомах,
вкажіть частинки, здатні до окиснення: а) +11 2 е ,8 е ; б) +11 2 е ,8 е 1 е ; в) +17
2 е ,8 е 7 е ; г) +17 2 е ,8 е 8 е ; д) +1 1 е ; е) +4 2 е ,2 е .
Завдання 8. Які з наведених схем зображують процеси відновлення:
2
0
0
1. Zn 2е Zn
1
7
0
4. 2 H 2е H 2
Чи
може
2
0
2. S 2е S
2
5. Mn 5е Mn
процес
відновлення
1
3. Na 1е Na
0
2
6. Mg 2е Mg
відбуватись
без
6
одночасного
7.
Завдання для підсумкової атестації (фрагмент)1.
2.
3.
4.
5.
6.
7.
СТУПІНЬ ОКИСНЕННЯ НІТРОГЕНУ В АМОНІЙ ХЛОРИДІ:
1. 0
2. +3
3. +5
4. –3
СПОЛУКА,
В
ЯКІЙ
НІТРОГЕН
МАЄ
НИЖЧИЙ
СТУПІНЬ
ОКИСНЕННЯ– ЦЕ:
1. НNО2
2. N2О 3. NН4Сl
4. NОF3.
В РЕЗУЛЬТАТІ ПЕРЕТВОРЕННЯ НNО3 → NО СТУПІНЬ ОКИСНЕННЯ
ОДНОГО
З
ЕЛЕМЕНТІВ
ЗНИЖУЄТЬСЯ
(ВІД
→
ДО):
1. +7 → +2
2. +4 → +2
3. +5 → –1
4. +5 → +2.
В РІВНЯННІ РЕАКЦІЇ NН3 + О2 → N2 + Н2О СУМА КОЕФІЦІЄНТІВ
ПЕРЕД ФОРМУЛАМИ ВИХІДНИХ РЕЧОВИН ДОРІВНЮЄ:
1. 4
2. 5
3. 6
4. 7
ЯКА ІЗ СПОЛУК ПРОЯВЛЯЄ ЛИШЕ ОКИСНІ ВЛАСТИВОСТІ?
1. Сульфатна кислота;
2. Сульфітна кислота;
3.
Сірководень;
4. Сірка.
–
ПЕРЕХІД Н2О2 → ОН – ЦЕ ПРОЦЕС:
1. Окиснення
2. Відновлення 3. Обмінний
ОДНАКОВИЙ СТУПІНЬ ОКИСНЕННЯ ХРОМУ В РЕЧОВИНАХ:
1) Nа3[Сr(ОН)6] і СrО3
2) СrО3 і NаСrО2
3) NаСrО2 і Сr2О3
4) Сr2О3 і К2СrО4
7
8.
Таблиця 3.8.2. Зведені результати тестування учнів 9 класівЧисло
правильно
виконаних
завдань
Результати тестування
Бал
менше 11
учнів
%
1–3
2
3,8
11-13
4–6
18
34,6
14-16
7–9
27
51,9
17-18
10–12
5
9,6
8
9.
• Доповідь закінчено. Дякую за увагу!9







 Химия
Химия








