Похожие презентации:
Карбоновые кислоты (карбоксильные производные)
1.
КАРБОНОВЫЕ КИСЛОТЫ(карбоксильные производные)
1
2.
• Классификация:- алифатические КК (предельные и непредельные)
- ароматические КК
- гетероциклические КК
-монокарбоновые кислоты (одноосновные)
- дикарбоновые (двухосновные)
-поликарбоновые
C
O
OH
Содержат карбоксильную группу,
связанную с алкильной или арильной группой
2
3.
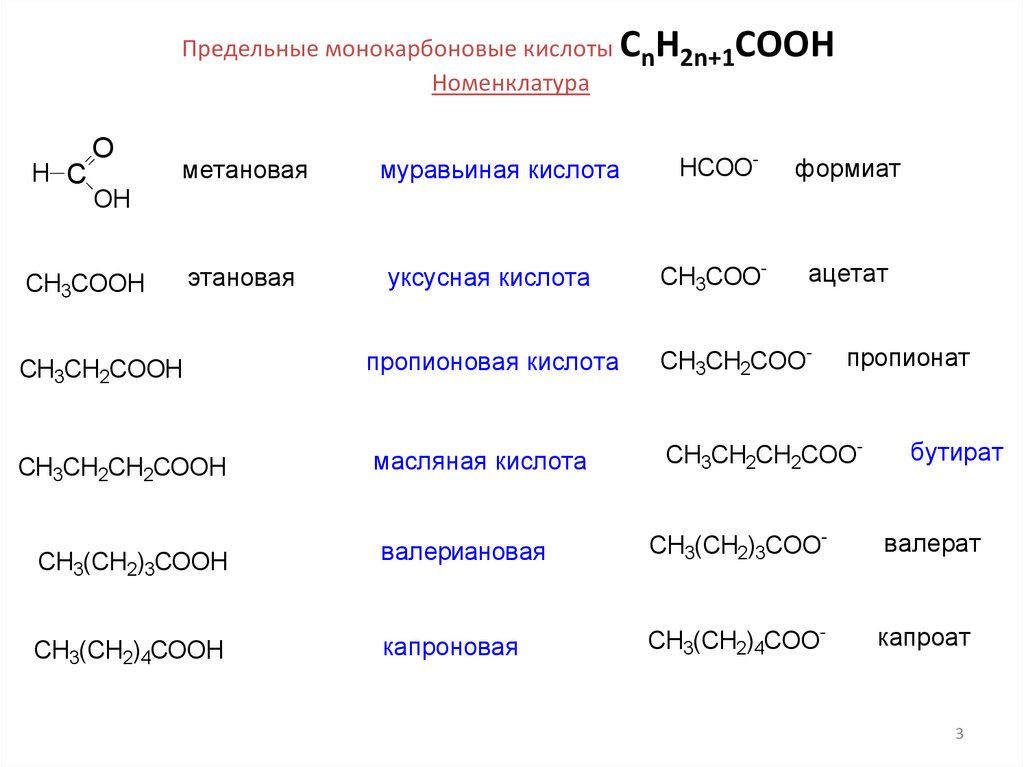
Предельные монокарбоновые кислоты CnH2n+1COOHНоменклатура
H C
O
метановая
муравьиная кислота
HCOO-
формиат
этановая
уксусная кислота
CH3COO-
ацетат
OH
CH3COOH
CH3CH2COOH
пропионовая кислота
CH3CH2COO-
CH3CH2CH2COOH
масляная кислота
CH3CH2CH2COO-
CH3(CH2)3COOH
валериановая
CH3(CH2)3COO-
валерат
CH3(CH2)4COOH
капроновая
CH3(CH2)4COO-
капроат
пропионат
бутират
3
4.
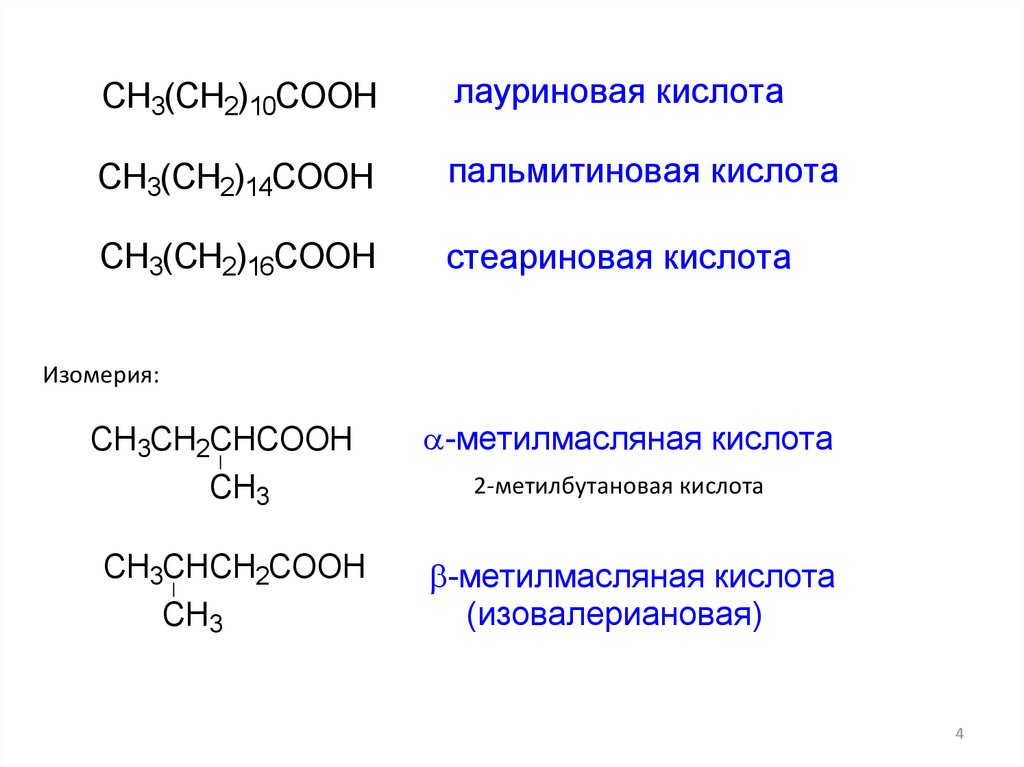
CH3(CH2)10COOHлауриновая кислота
CH3(CH2)14COOH
пальмитиновая кислота
CH3(CH2)16COOH
стеариновая кислота
Изомерия:
CH3CH2CHCOOH
CH3
-метилмасляная кислота
CH3CHCH2COOH
CH3
-метилмасляная кислота
(изовалериановая)
2-метилбутановая кислота
4
5.
Строение карбоксильной группыГруппа плоская
lC=O = 0,124 нм
lC-O = 0,131нм
lO-H = 0,095 нм
Сдвиг электронов к карбонильному атому кислорода
приводит к некоторому гашению положительного заряда
на атоме углерода, поэтому группа С=О в кислотах
не склонна к реакциям присоединения.
Поскольку электронная плотность на атоме
кислорода ОН-группы уменьшается, связь О-Н ослабевает,
И атом водорода легко отщепляется.
5
6.
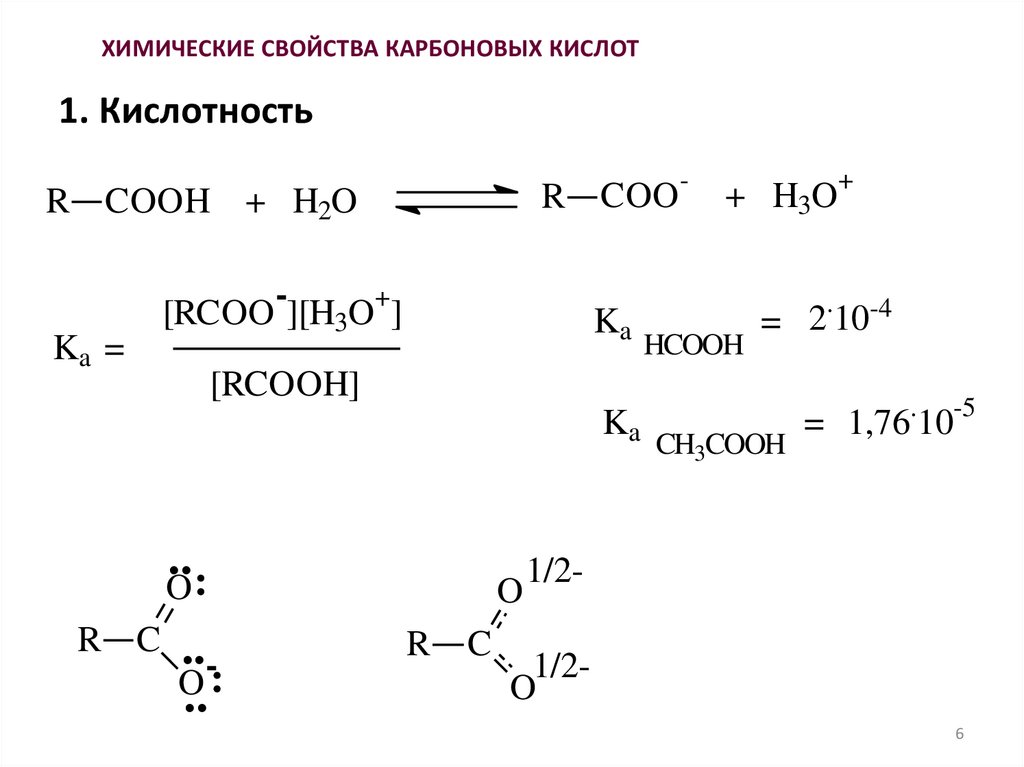
ХИМИЧЕСКИЕ СВОЙСТВА КАРБОНОВЫХ КИСЛОТ1. Кислотность
R COO
R COOH + H2O
Ka =
+
[RCOO ][H3O ]
Ka
-
+ H3O
.
HCOOH
= 2 10-4
[RCOOH]
Ka
..
O
R C ..
O
..
O
R
C
+
.
CH3COOH
= 1,76 10
-5
1/2-
1/2O
6
7.
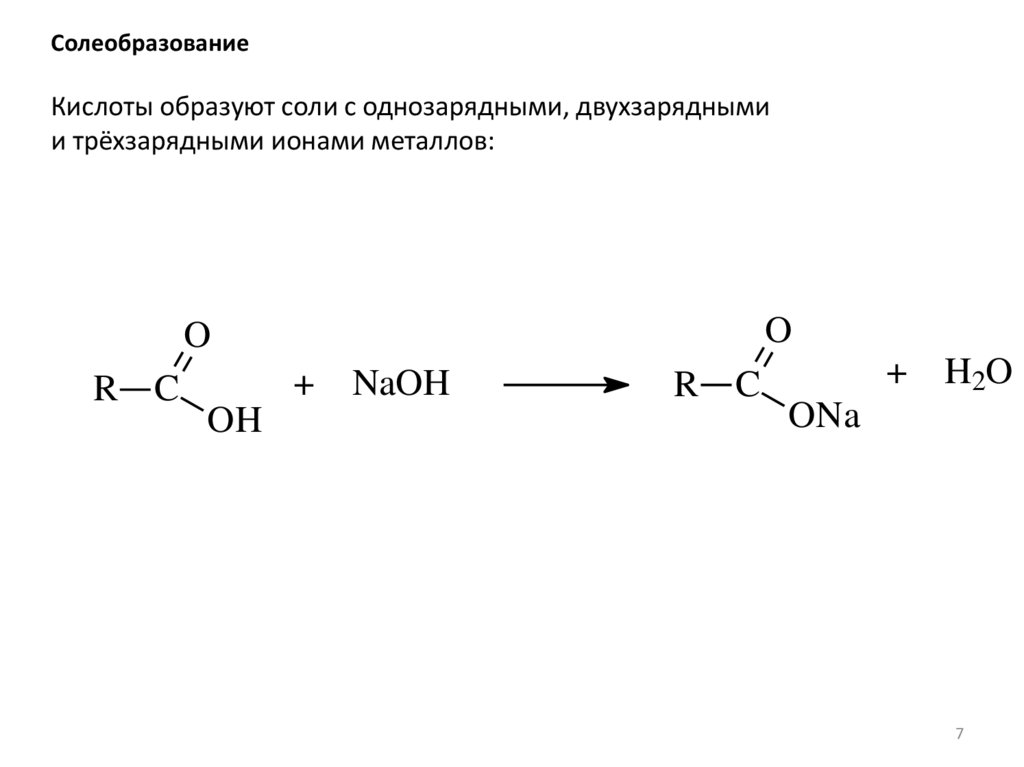
СолеобразованиеКислоты образуют соли с однозарядными, двухзарядными
и трёхзарядными ионами металлов:
O
O
R C
+ NaOH
OH
R C
+ H2O
ONa
7
8.
2. Реакции нуклеофильного замещенияв карбоксильной группе -получение функциональных производных карбоновых кислот (OH-группа
замещена на группы NH2, OR, OC(O)R, Cl).
Все они содержат ацильную группу
R C
O
ацильная группа
ФПКК можно превращать друг в друга, а гидролизом снова превратить в кислоту.
8
9.
ФУНКЦИОНАЛЬНЫЕ ПРОИЗВОДНЫЕКАРБОНОВЫХ КИСЛОТ (ФПКК)
9
10.
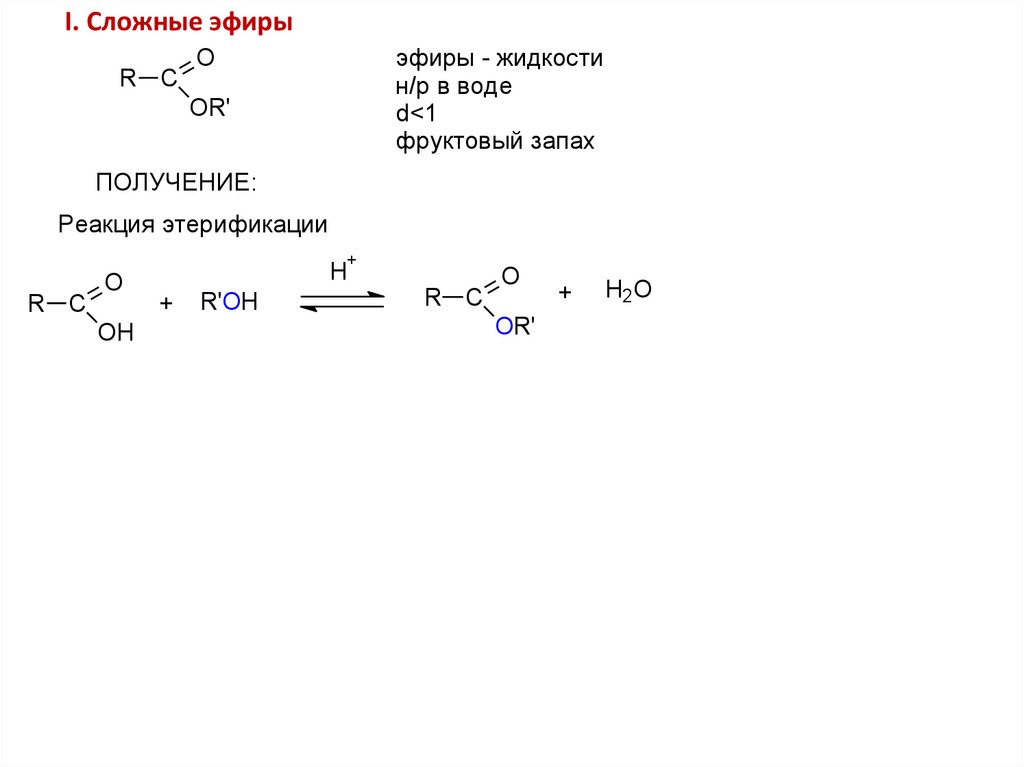
I. Сложные эфирыR C
эфиры - жидкости
н/р в воде
d<1
фруктовый запах
O
OR'
ПОЛУЧЕНИЕ:
1). Реакция этерификации
+
R C
O
H
+
OH
Катализаторы:
H2SO4 (конц.),
HCl (сухой газ)
R'OH
R C
O
+
H2O
OR'
Минеральные кислоты ускоряют прямую и обратную реакции,
протонируя кислород карбонильной группы и тем самым
увеличивая склонность углерода карбонильной группы
к присоединению нуклеофила.
Процесс равновесный.
Для смещения равновесия: избыток спирта; удаление H2.O
Опыты с кислотой, меченой по 18O, показали,
что в составе H2O18 выделяется OH-группа кислоты.
По реакционной способности:
первичный спирт > вторичный спирт > третичный спирт
10
11.
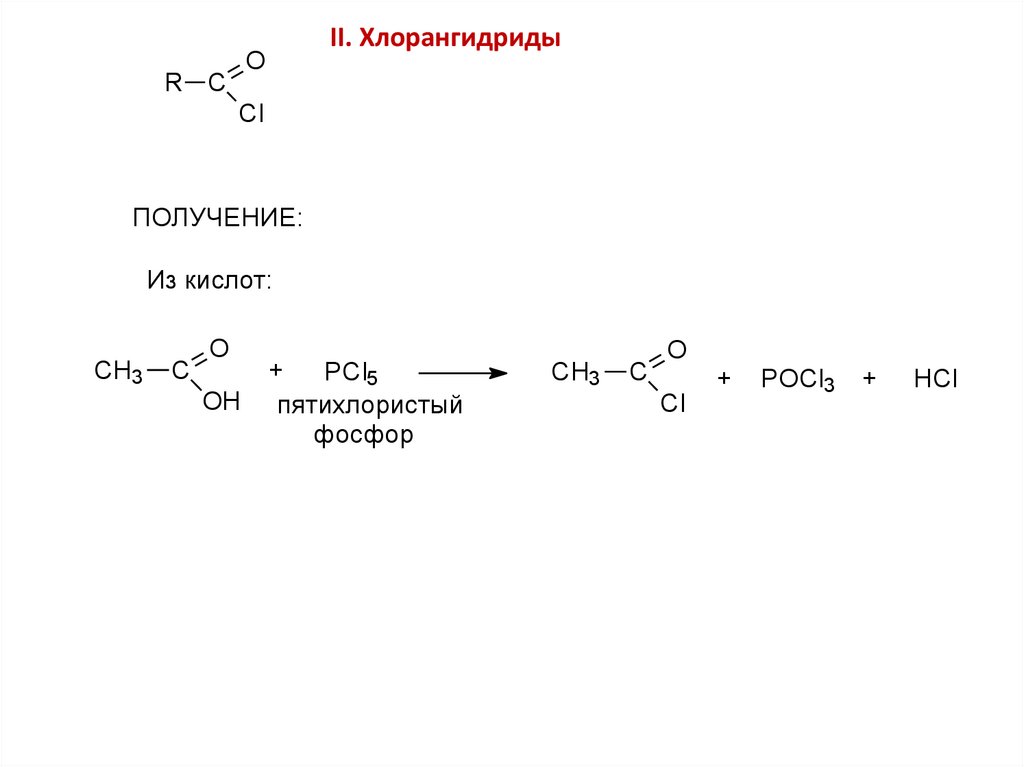
II. ХлорангидридыO
R C
Cl
ПОЛУЧЕНИЕ:
1) Из кислот:
CH3
C
O
OH
CH3
C
O
+
PCl5
пятихлористый
фосфор
+
OH
COCl2
фосген
C
O
+
POCl3
+
CO2
Cl
CH3
C
O
Cl
+
HCl
+
HCl
SO2
+
O
O
C
C
OH
CH3
+
SOCl2
Cl
+
HCl
тионилхлорид
11
12.
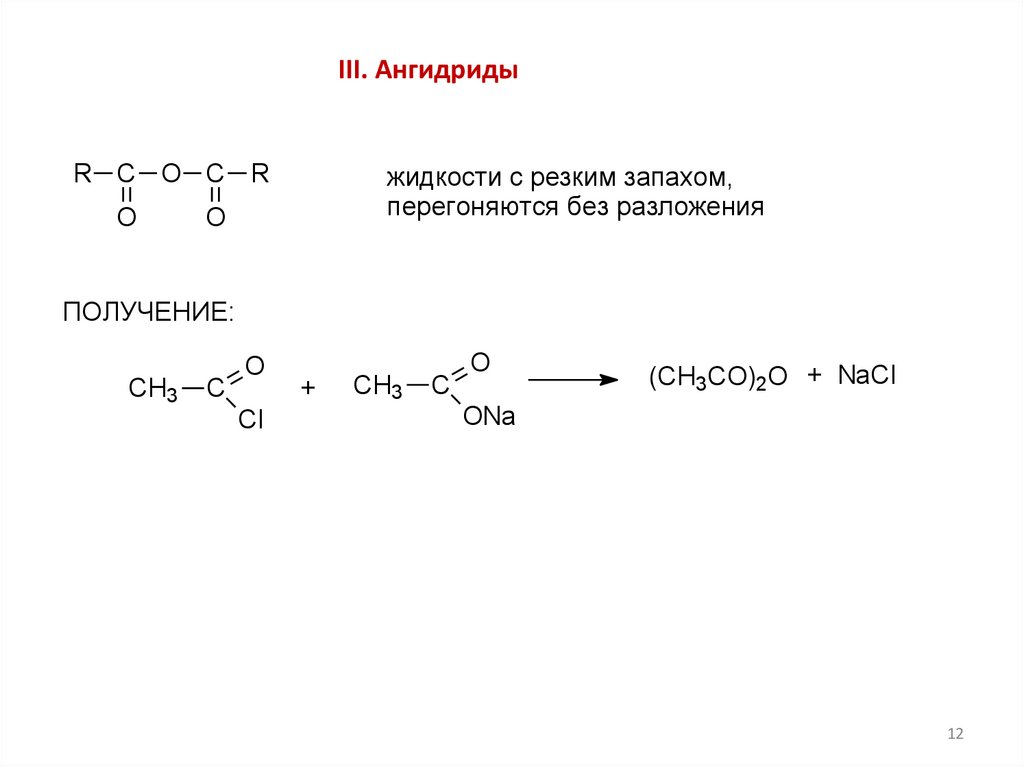
III. АнгидридыR C O C R
O
жидкости с резким запахом,
перегоняются без разложения
O
ПОЛУЧЕНИЕ:
1)
CH3
C
O
+
CH3
C
C O
кетен
(CH3CO)2O + NaCl
ONa
Cl
2) CH2
O
+
CH3
C
O
(CH3CO)2O
OH
Кетен получают высокотемпературной дегидратацией
уксусной кислоты или пиролизом ацетона
12
13.
IV. АмидыR C
O
NH2
ПОЛУЧЕНИЕ:
Из аммонийных солей карбоновых кислот:
R C
O
2200C
ONH4
в токе NH3
R C
O
+
H 2O
NH2
13
14.
Липидысодержатся в животных и растительных
тканях
Большая группа соединений, содержащих в
своем составе сложно-эфирную связь,
нерастворимых в воде и выполняющих в
организме ряд важных функций
14
15.
Структурные компоненты липидов• СПИРТЫ
• ВЫСШИЕ ЖИРНЫЕ КАРБОНОВЫЕ КИСЛОТЫ
• другие вещества
15
16.
Липидыпростые
СПИРТЫ
ВЫСШИЕ ЖИРНЫЕ КК
сложные
СПИРТЫ
ВЫСШИЕ ЖИРНЫЕ КК
другие вещества
16
17.
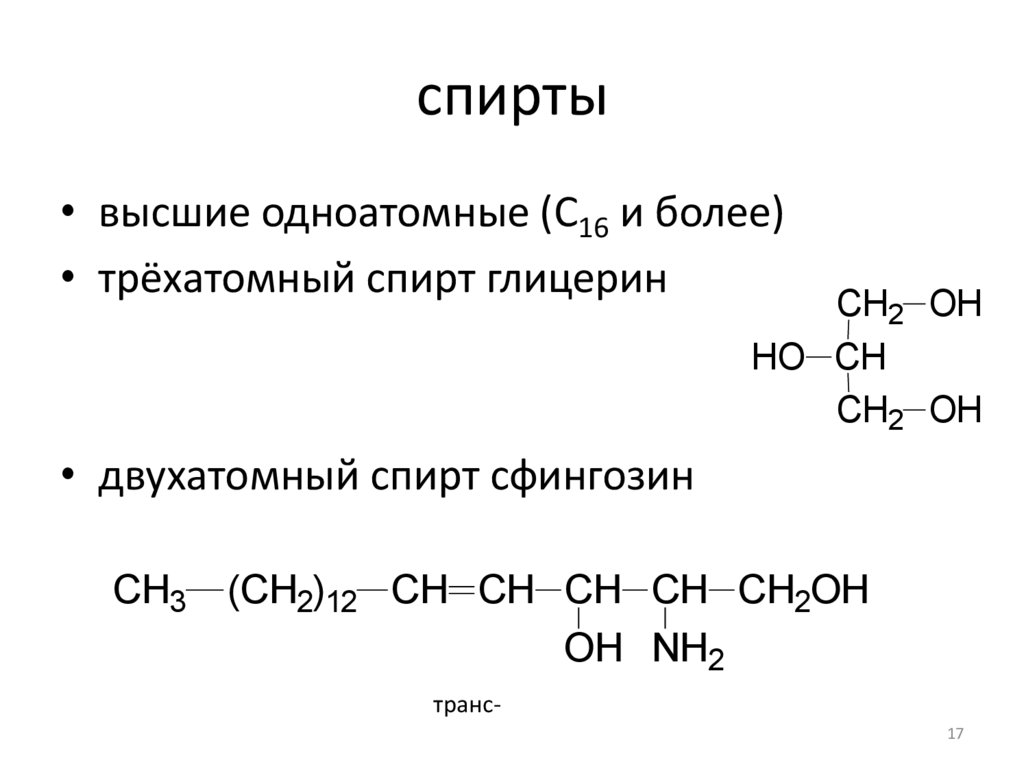
спирты• высшие одноатомные (С16 и более)
• трёхатомный спирт глицерин
CH2 OH
HO CH
CH2 OH
• двухатомный спирт сфингозин
CH3 (CH2)12 CH CH CH CH CH2OH
OH NH2
транс17
18.
Простые липиды• воски
• жиры и масла
• церамиды
• стериды
18
19.
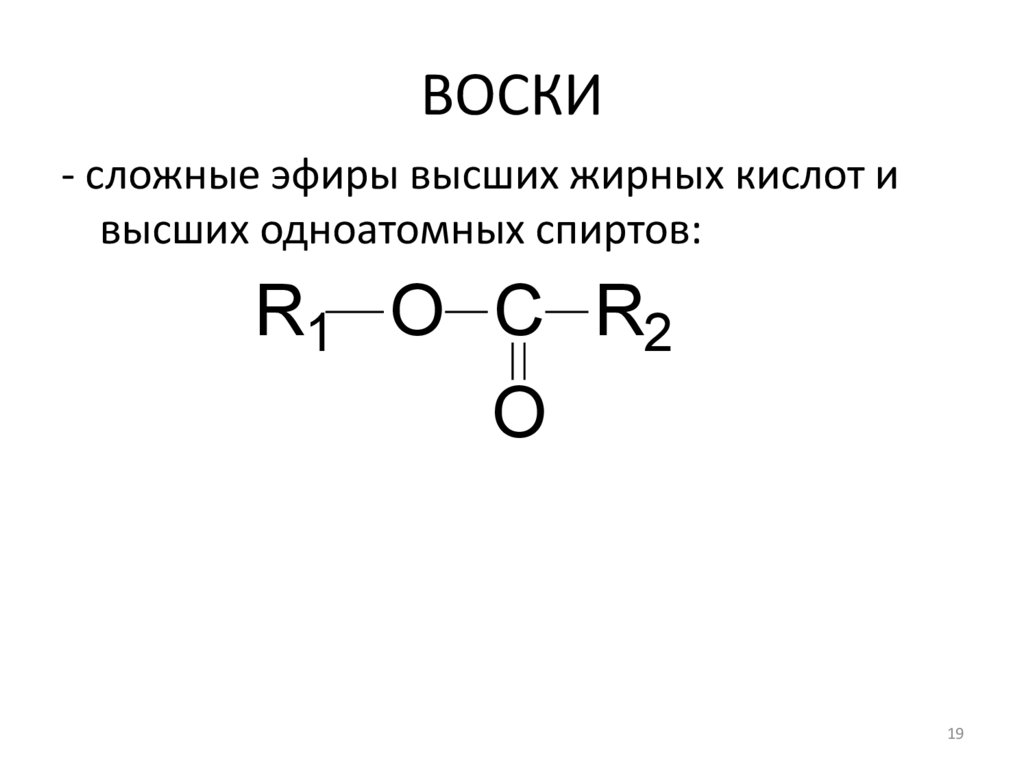
ВОСКИ- сложные эфиры высших жирных кислот и
высших одноатомных спиртов:
R1 O C R2
O
19
20.
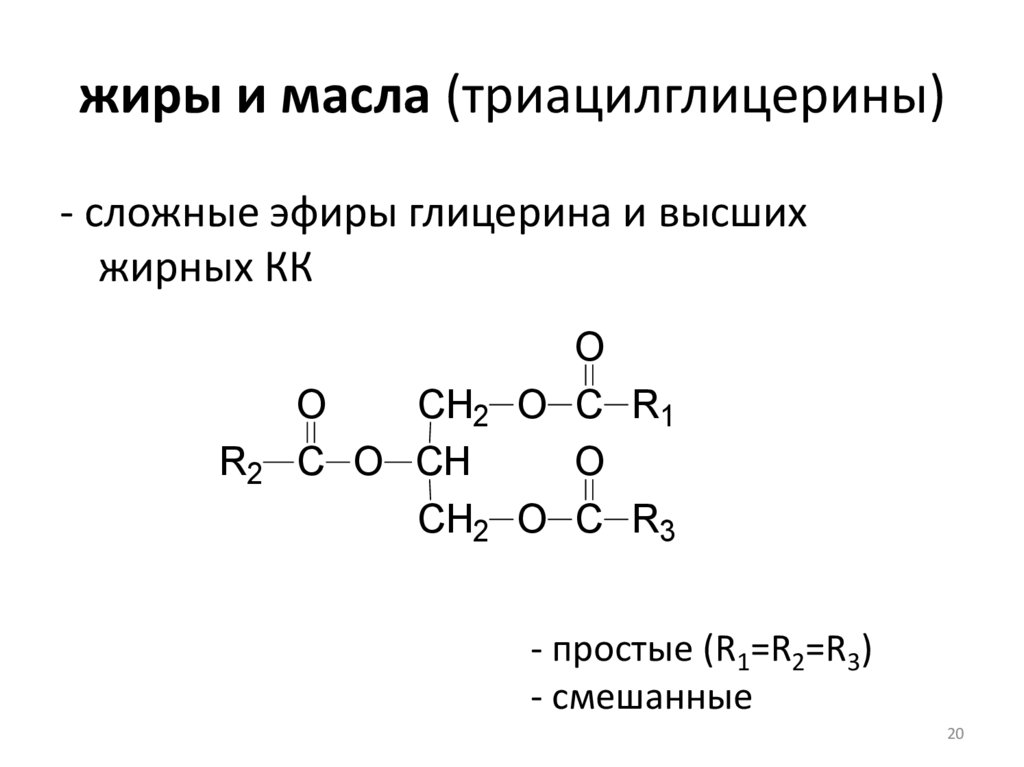
жиры и масла (триацилглицерины)- сложные эфиры глицерина и высших
жирных КК
R2
O
O
CH2 O C R1
C O CH
O
CH2 O C R3
- простые (R1=R2=R3)
- смешанные
20
21.
церамиды- N-ацилированные производные спирта
сфингозина
21
22.
стериды- сложные эфиры высокосмолекулярного
циклического спирта стерола и
высокомолекулярной КК
22
23.
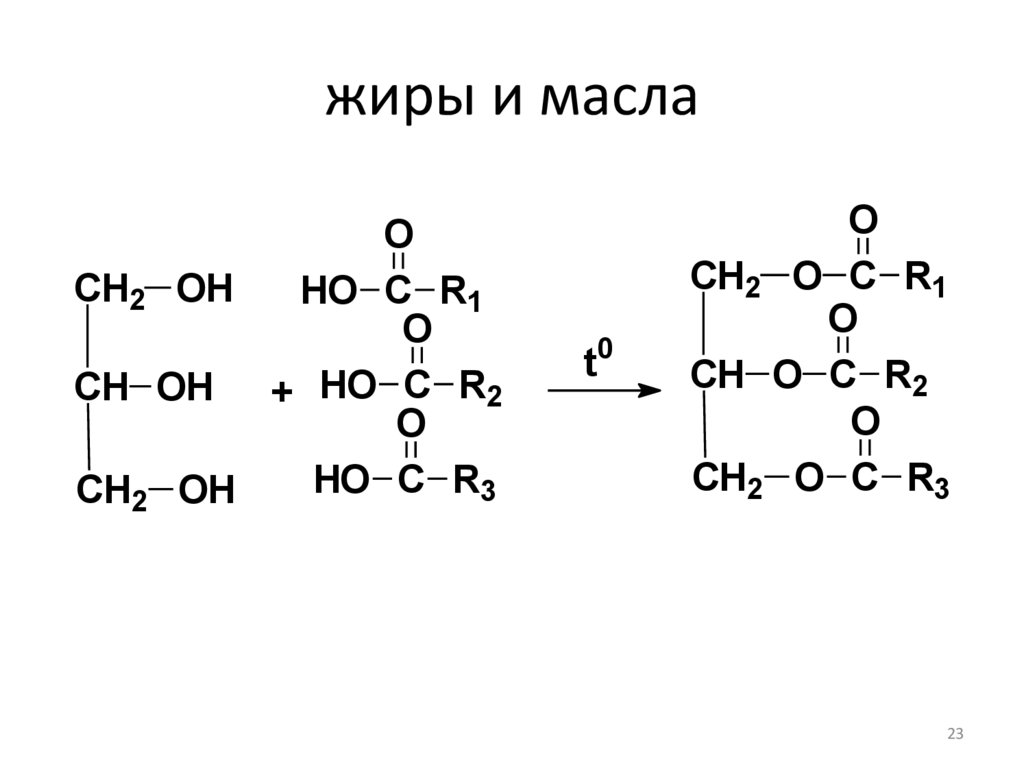
жиры и маслаO
CH2 OH
HO C R1
O
CH OH + HO C R2
O
HO C R3
CH2 OH
t0
O
CH2 O C R1
O
CH O C R2
O
CH2 O C R3
23
24.
OCH2 O C C17H35
O
CH O C C17H35
O
CH2 O C C17H35
тристеарин
(тристеароилглицерин)
O
CH2 O C C17H33
O
CH O C C17H33
O
CH2 O C C17H33
триолеин
(триолеилглицерин)
24
25.
OCH2 O C C17H33
O
CH O C C15H31
O
CH2 O C C17H35
1-олео-2-пальмитостеарин
(1-олеоил-2-пальмитоил-3-стеароилглицерин)
25
26.
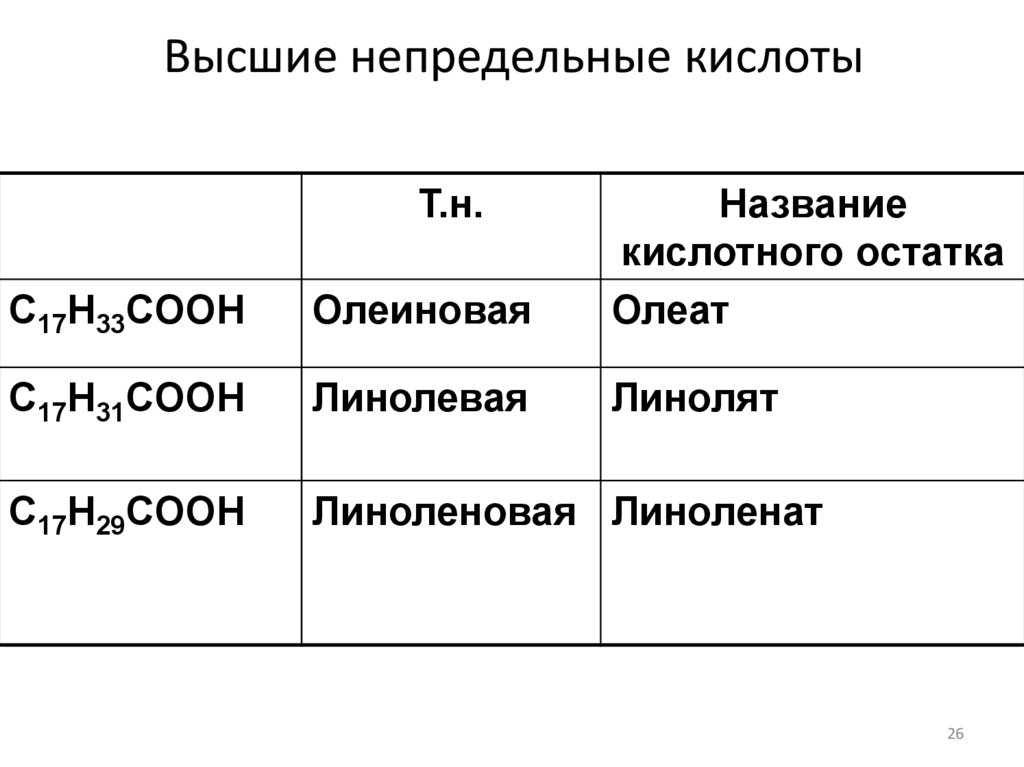
Высшие непредельные кислотыТ.н.
C17H33COOH
Олеиновая
Название
кислотного остатка
Олеат
C17H31COOH
Линолевая
Линолят
C17H29COOH
Линоленовая Линоленат
26
27.
химические свойства- гидрогенизация
O
CH2 O C C17H33
O
CH O C C17H33
O
CH2 O C C17H33
t0
+ 3H2
kat
O
CH2 O C C17H35
O
CH O C C17H35
O
CH2 O C C17H35
27
28.
- непредельные кислоты в составе жира обесцвечиваютраствор KMnO4, вступают в реакции присоединения,
например, галогенов
• Иодное число – мера ненасыщенности
триацилглицеринов. Оно соответствует массе (г)
иода, которое может присоединиться к 100 г
вещества.
жир
сливочное масло
жир человека
подсолнечное масло
иодное число
30
64
130
28
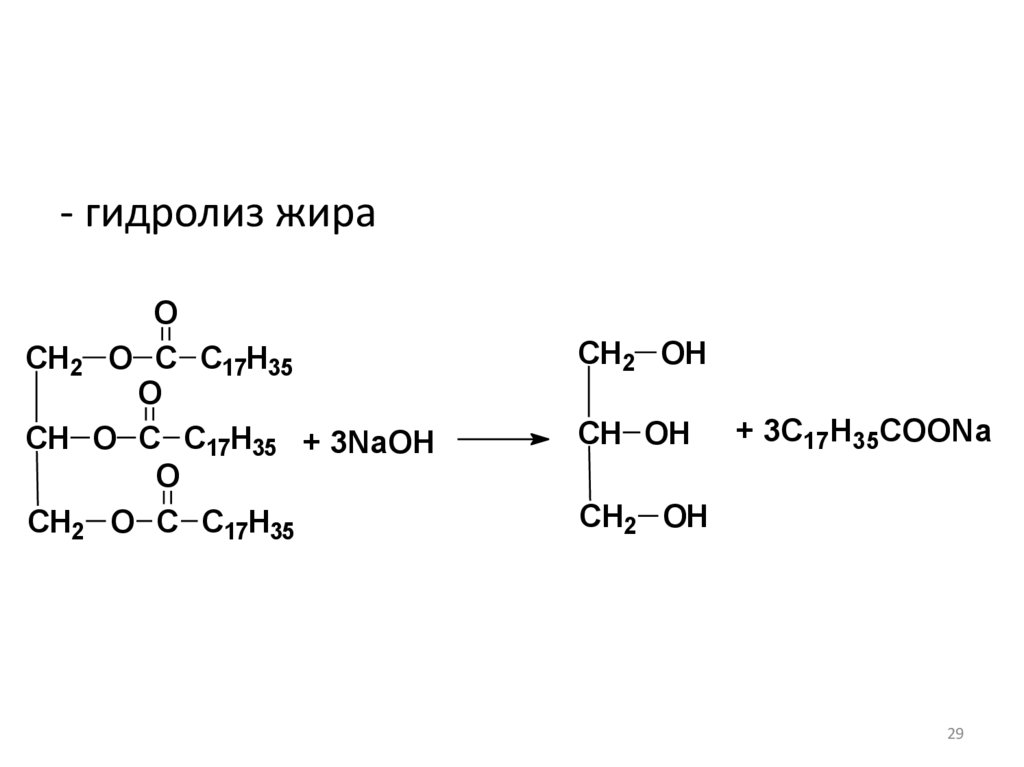
29.
- гидролиз жираO
CH2 O C C17H35
O
CH O C C17H35 + 3NaOH
O
CH2 O C C17H35
CH2 OH
CH OH
+ 3C17H35COONa
CH2 OH
29
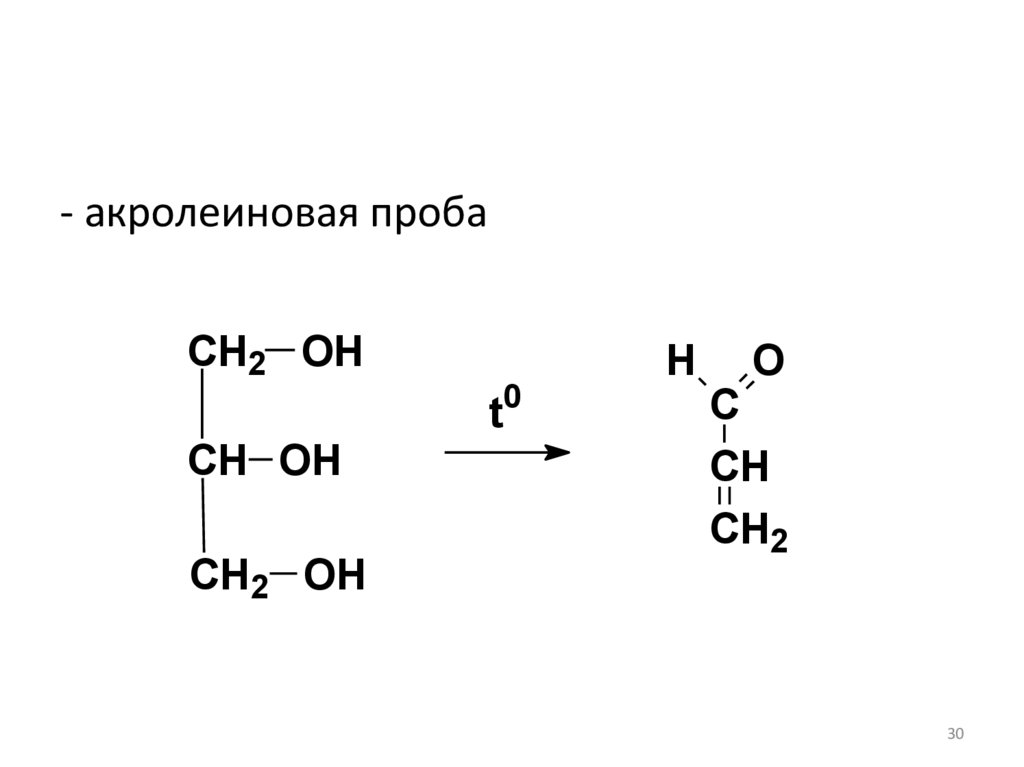
30.
- акролеиновая пробаCH2 OH
H
0
t
CH OH
CH2 OH
O
C
CH
CH2
30
31.
Биологическая роль жиров• Энергетическая
• Структурная
• Резервная
• Механическая защита внутренних органов
от повреждений
• Термоизоляционная
• Источник эндогенной воды
• Растворяют жирорастворимые витамины
(A,D,E,K)
31
32.
Сложные липиды• Фосфолипиды
• Сфинголипиды
• Гликолипиды
32
33.
Фосфолипиды- липиды, при гидролизе отщепляющие
фосфорную кислоту
Глицерофосфолипиды - сложные эфиры
глицерина с высшими жирными кислотами
и фосфорной кислотой.
В состав фосфолипидов входят также
азотсодержащие соединения, такие как
холин, этаноламин или серин.
33
34.
• Глицерофосфолипиды – главныелипидные компоненты клеточных
мембран. Они сопутствуют жирам в пище
и служат источником фосфорной кислоты,
необходимой для жизни человека.
34
35.
• Глицерофосфолипиды являютсяпроизводными фосфатидной кислоты. В их
состав входят глицерин, жирные кислоты,
фосфорная кислота и обычно
азотсодержащие соединения.
R2
O
O
CH2 O C R1
C O CH
O
CH2 O P OH
OH
фосфатидная кислота
35
36.
глицерофосфолипидR2
O
CH2 O C R1
O
O
C O CH
CH2 O P O R3
O
Как правило, в положении 1 – остаток насыщенной, а в положении 2 – остаток
ненасыщенной кислоты
36
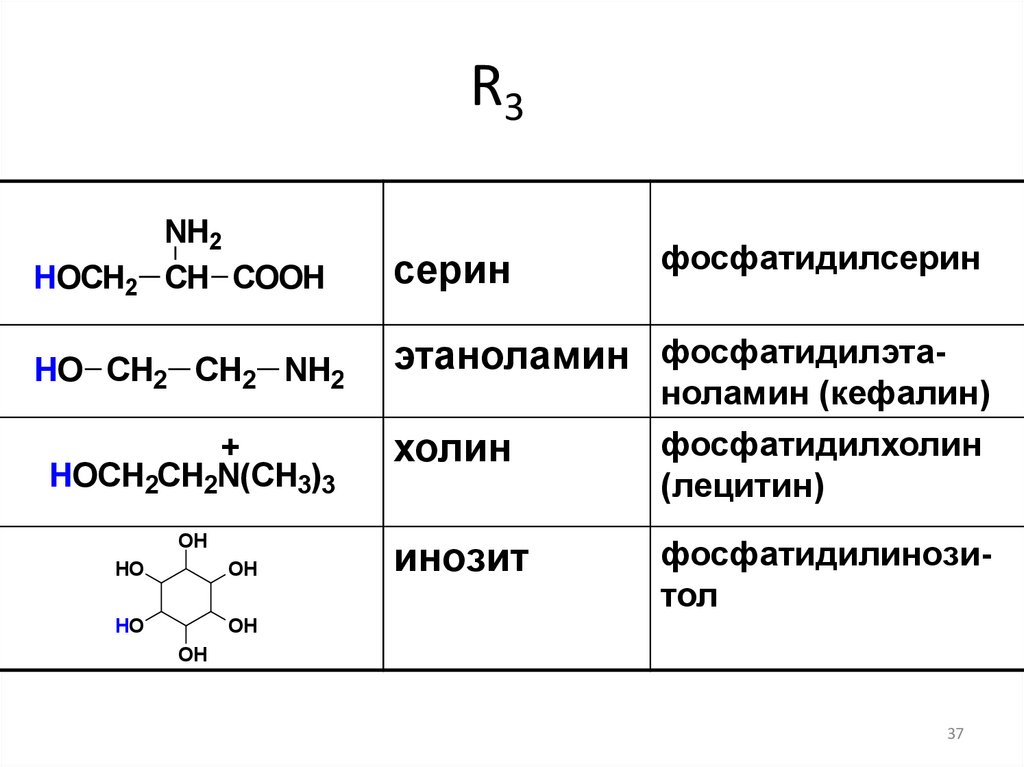
37.
R3HOCH2
NH2
CH COOH
HO CH2 CH2 NH2
серин
фосфатидилсерин
этаноламин фосфатидилэта-
+
HOCH2CH2N(CH3)3
холин
ноламин (кефалин)
фосфатидилхолин
(лецитин)
OH
инозит
фосфатидилинозитол
HO
OH
HO
OH
OH
37
38.
OCH2 O C R1
O
+
+ HOCH2CH2N(CH3)3
CH O C R2
- H2O
O
CH2 O P O H
O-
O
CH2 O C R1
.
O
CH O C R2
O
+
OCH
CH
N(CH
CH2 O P
2
2
3)3
O-
лецитин
Из всех липидов глицерофосфолипиды обладают
полярными свойствами. При помещении
глицерофосфолипидов в воду в истинный раствор
переходит лишь небольшая их часть, основная же
масса липидов находится в виде мицелл.
38
39.
Биологическая роль фосфолипидов• Структурная - входят в состав клеточных
мембран
• Повышают растворимость холестерина и
способствуют его выведению из организма
• Препятствуют синтезу жира в печени
39
























 Химия
Химия








