Похожие презентации:
mnogoatomnye_spirty_i_fenoly
1.
Кроссворд1г
е кс а н
2м е т и л б е н з о л
3а л к и н ы
4ц и к л о г е к с а н
5а л к е н ы
6б р о м э т а н
7э т и л а т
8м а р к о в н и к о в
По горизонтали:
1. Из какого алкана можно получить бензол. 2. Продукт реакции бензола с
метилхлоридом. 3. Класс углеводородов, содержащих тройную связь. 4. Продукт
реакции бензола с водородом. 5. К какому классу соединений относится 2метилпентен-2. 6. Продукт реакции этена с бромоводородом. 7. Какая соль
образуется при взаимодействии натрия с этанолом.
8. Ученый,
сформулировавший правило, по которому протекает реакция 2-метилбутен-1 с
бромоводородом.
По вертикали:
1. Трехатомный спирт.
2.
Тема урокаМногоатомные спирты.
Фенолы
3.
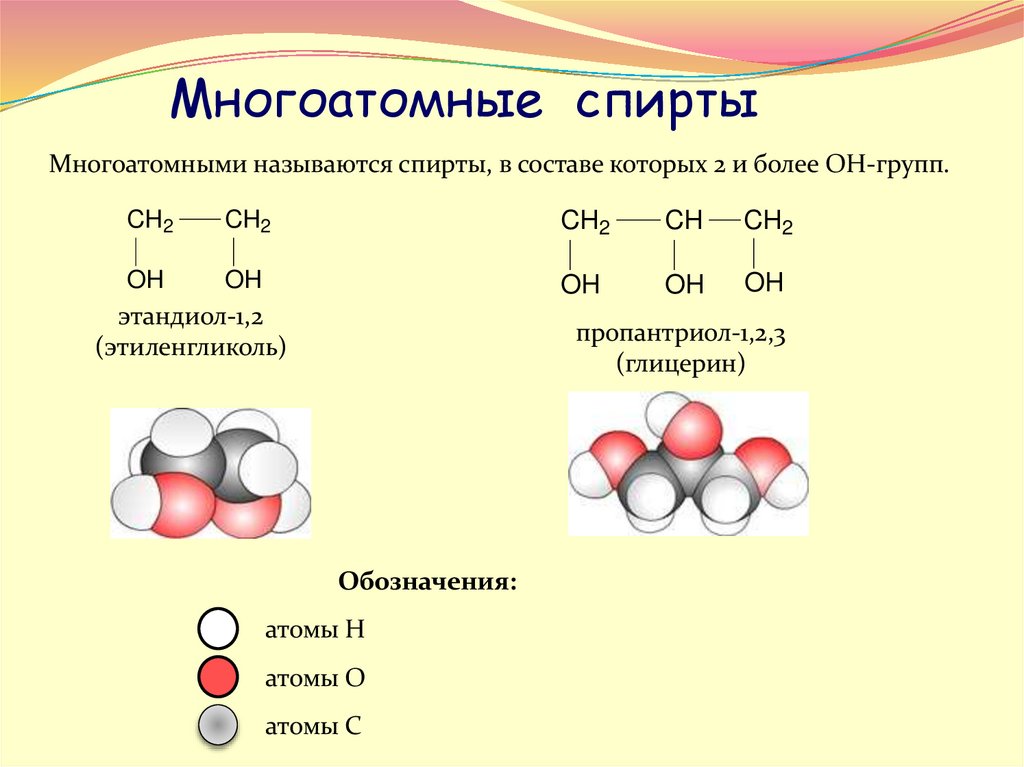
Многоатомные спиртыМногоатомными называются спирты, в составе которых 2 и более ОН-групп.
CH2
CH2
CH2
CH
CH2
OH
OH
этандиол-1,2
(этиленгликоль)
OH
OH
OH
пропантриол-1,2,3
(глицерин)
Обозначения:
атомы Н
атомы О
атомы С
4.
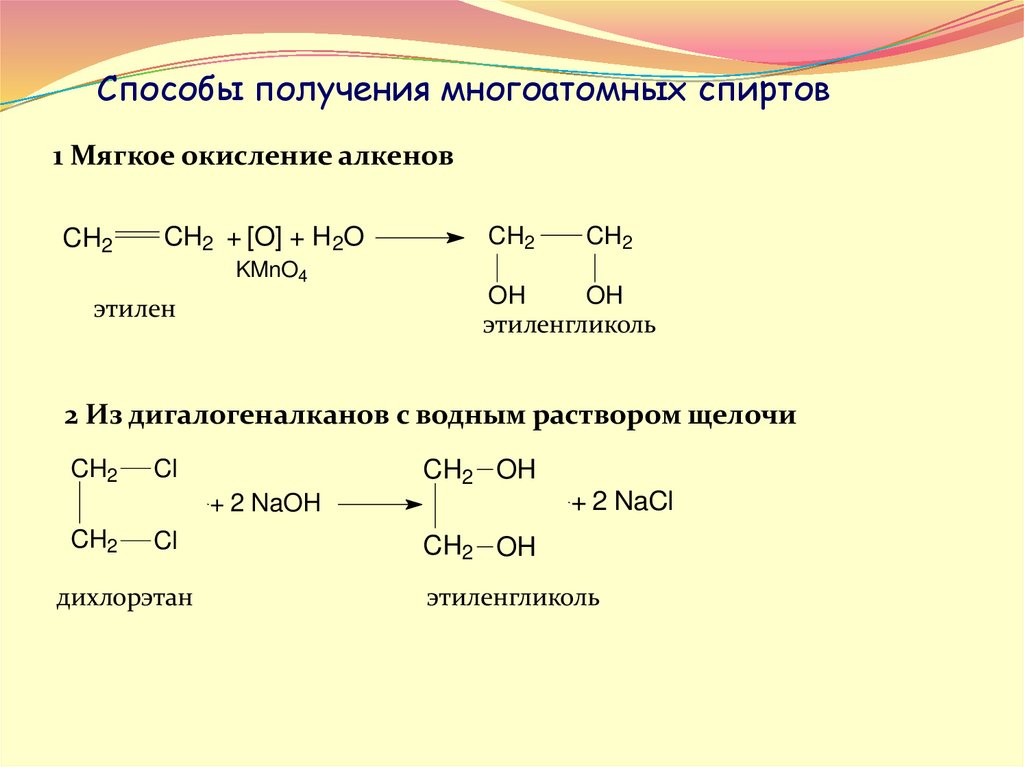
Способы получения многоатомных спиртов1 Мягкое окисление алкенов
CH2
CH2 + [O] + H 2O
CH2
CH2
KMnO4
OH
OH
этиленгликоль
этилен
2 Из дигалогеналканов с водным раствором щелочи
CH2
Cl
CH2 OH
+ 2 NaCl
+ 2 NaOH
CH2
Cl
дихлорэтан
CH2 OH
этиленгликоль
5.
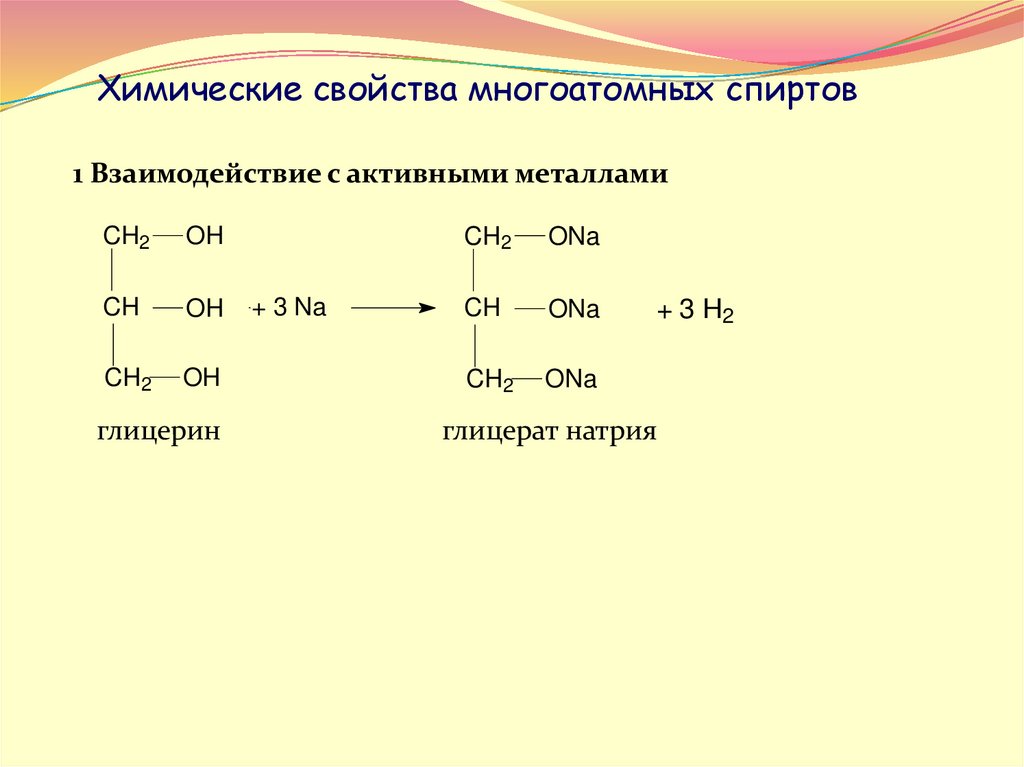
Химические свойства многоатомных спиртов1 Взаимодействие с активными металлами
CH2
OH
CH
OH
CH2
OH
глицерин
+ 3 Na
CH2
ONa
CH
ONa
CH2
ONa
+ 3 H2
глицерат натрия
6.
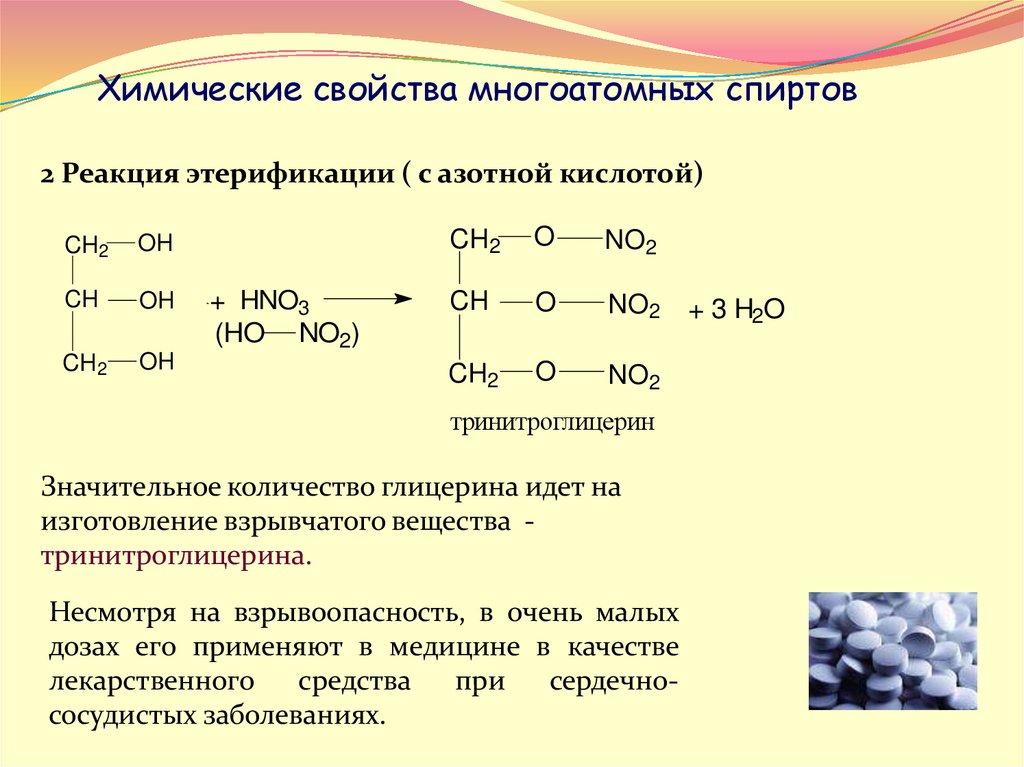
Химические свойства многоатомных спиртов2 Реакция этерификации ( с азотной кислотой)
CH2
OH
CH
OH
CH2
OH
+ HNO3
(HO NO2)
CH2
O
NO2
CH
O
NO2
CH2
O
NO2
тринитроглицерин
Значительное количество глицерина идет на
изготовление взрывчатого вещества тринитроглицерина.
Несмотря на взрывоопасность, в очень малых
дозах его применяют в медицине в качестве
лекарственного
средства
при
сердечнососудистых заболеваниях.
+ 3 H2O
7.
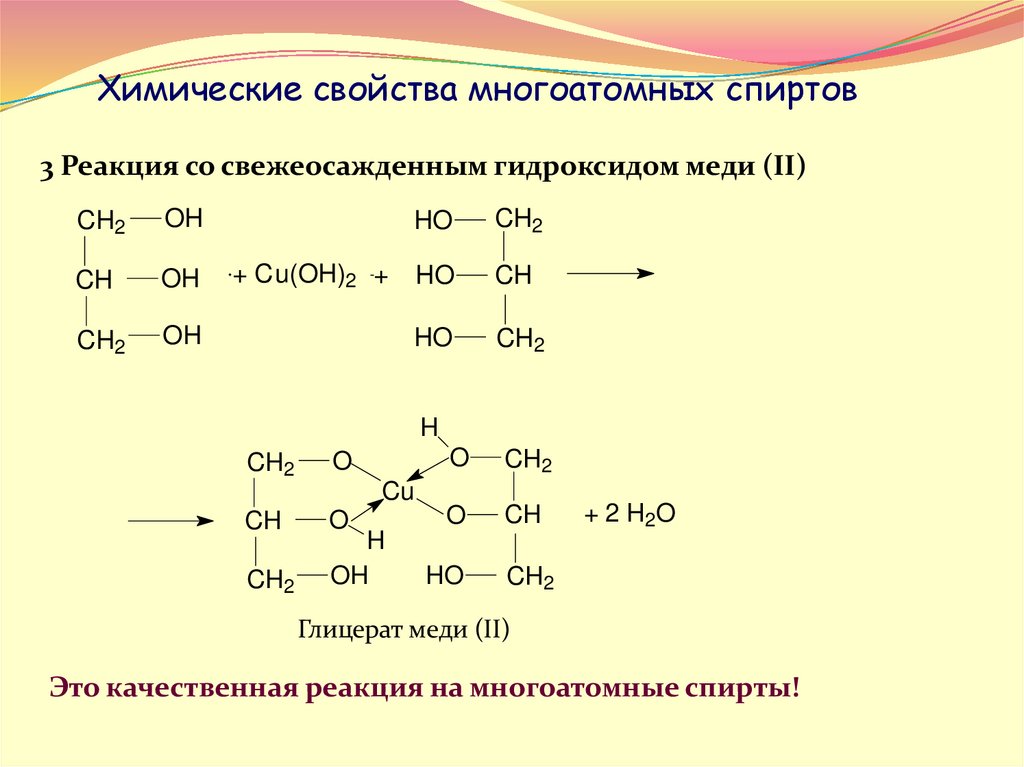
Химические свойства многоатомных спиртов3 Реакция со свежеосажденным гидроксидом меди (II)
CH2
OH
CH
OH
CH2
OH
HO
CH2
HO
CH
HO
CH2
+ Cu(OH)2 +
H
CH2
O
O
CH2
O
CH
HO
CH2
Cu
CH
CH2
O
H
OH
+ 2 H2O
Глицерат меди (II)
Это качественная реакция на многоатомные спирты!
8.
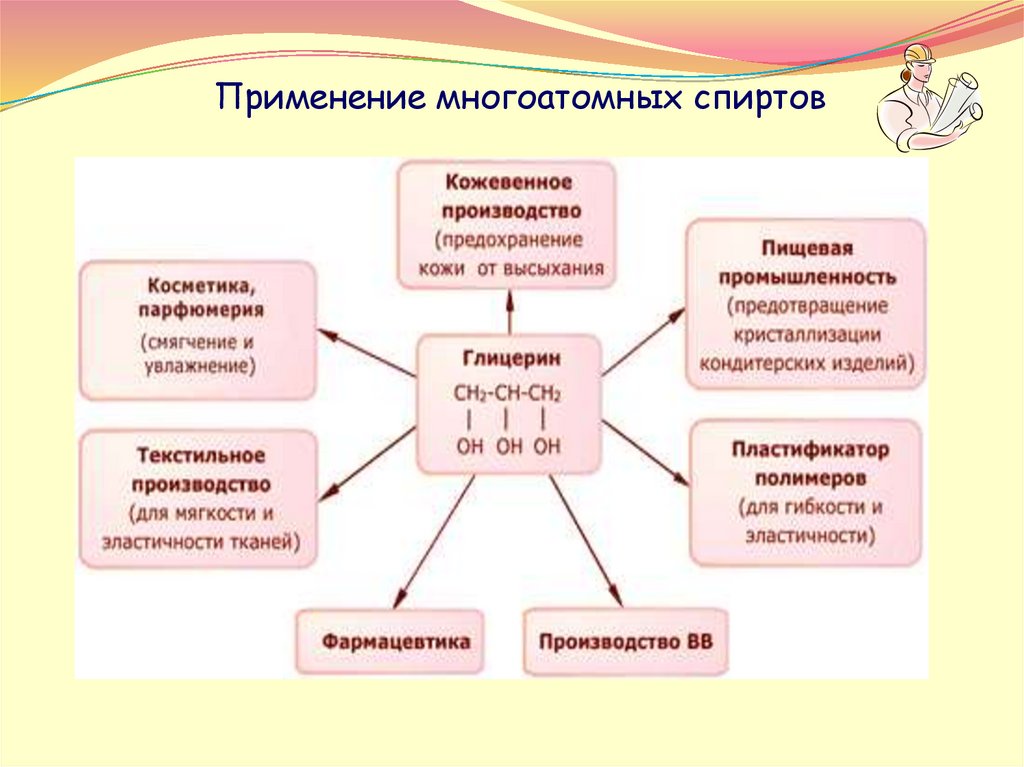
Применение многоатомных спиртов9.
Применение многоатомных спиртов10.
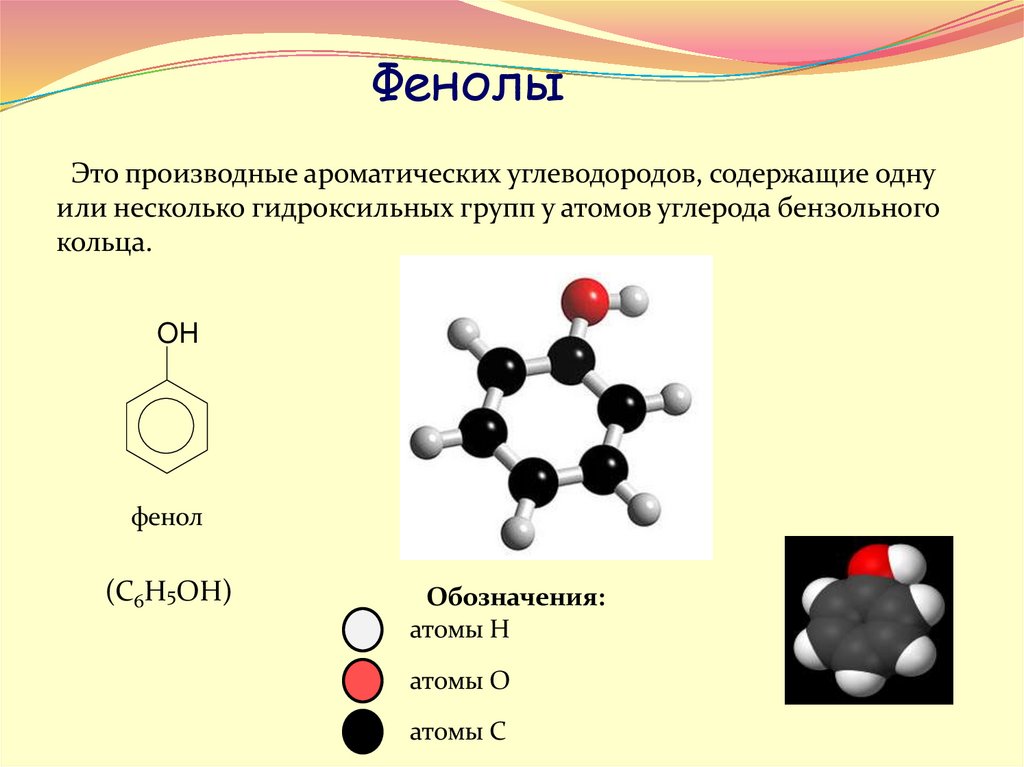
ФенолыЭто производные ароматических углеводородов, содержащие одну
или несколько гидроксильных групп у атомов углерода бензольного
кольца.
OH
фенол
(С6Н5ОН)
Обозначения:
атомы Н
атомы О
атомы С
11.
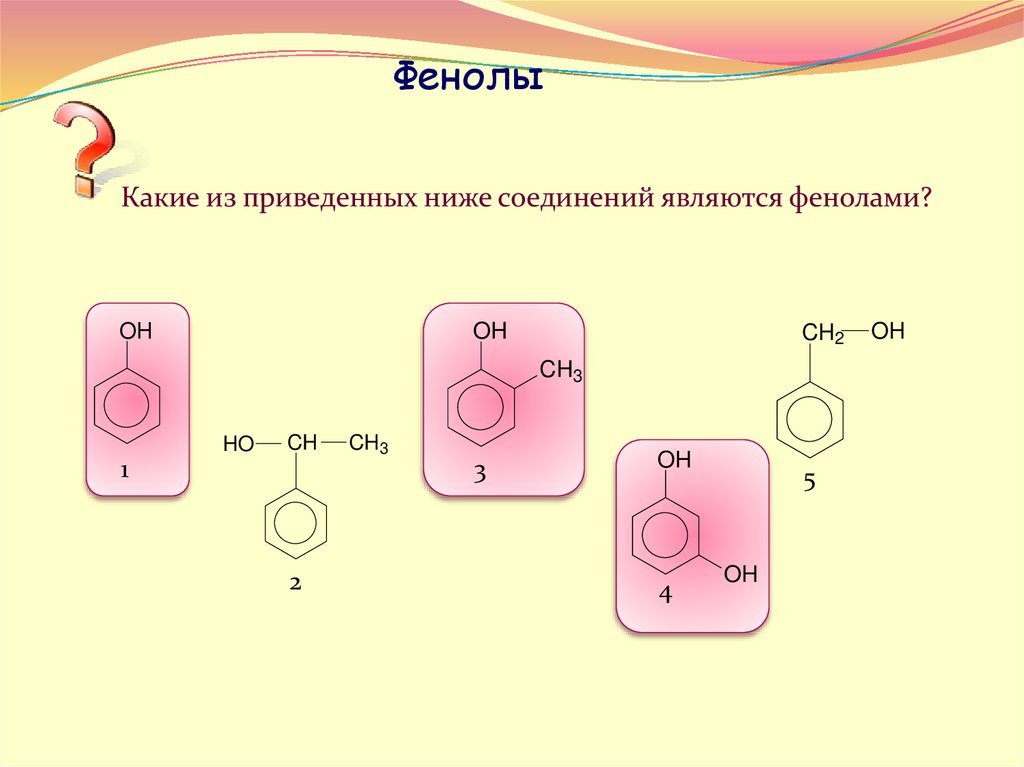
ФенолыКакие из приведенных ниже соединений являются фенолами?
OH
OH
CH2
CH3
HO
CH
1
CH3
3
2
OH
4
5
OH
OH
12.
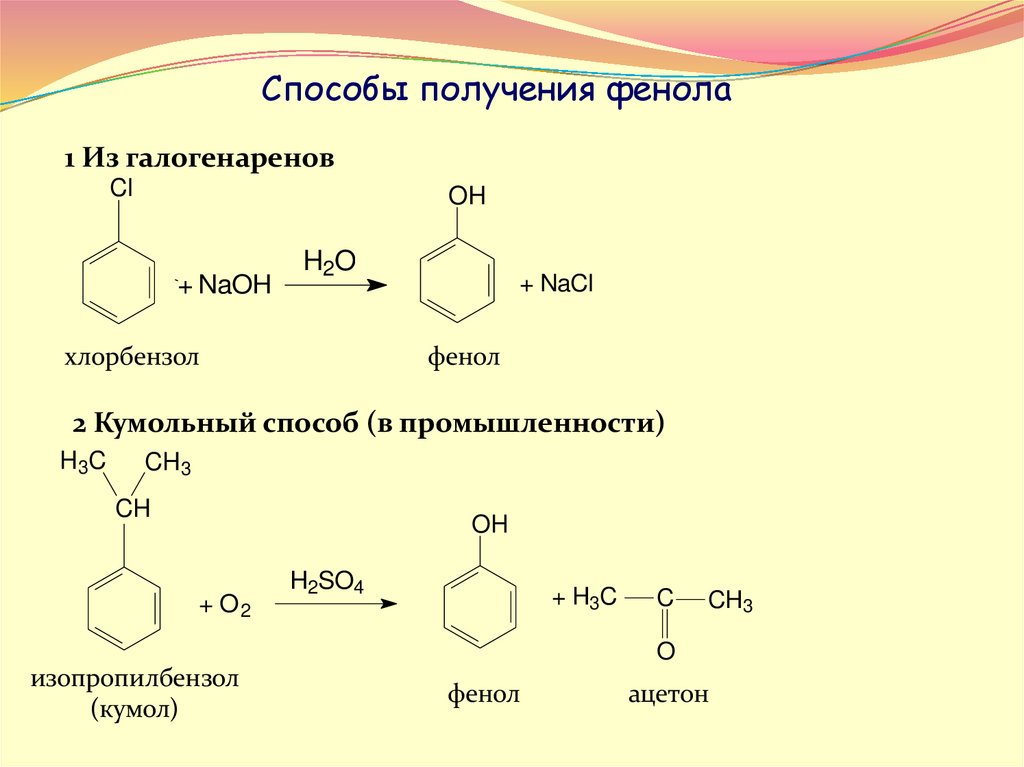
Способы получения фенола1 Из галогенаренов
Cl
OH
+ NaOH
H2O
хлорбензол
+ NaCl
фенол
2 Кумольный способ (в промышленности)
H 3C
CH3
CH
OH
+ O2
H2SO4
+ H3C
C
CH3
O
изопропилбензол
(кумол)
фенол
ацетон
13.
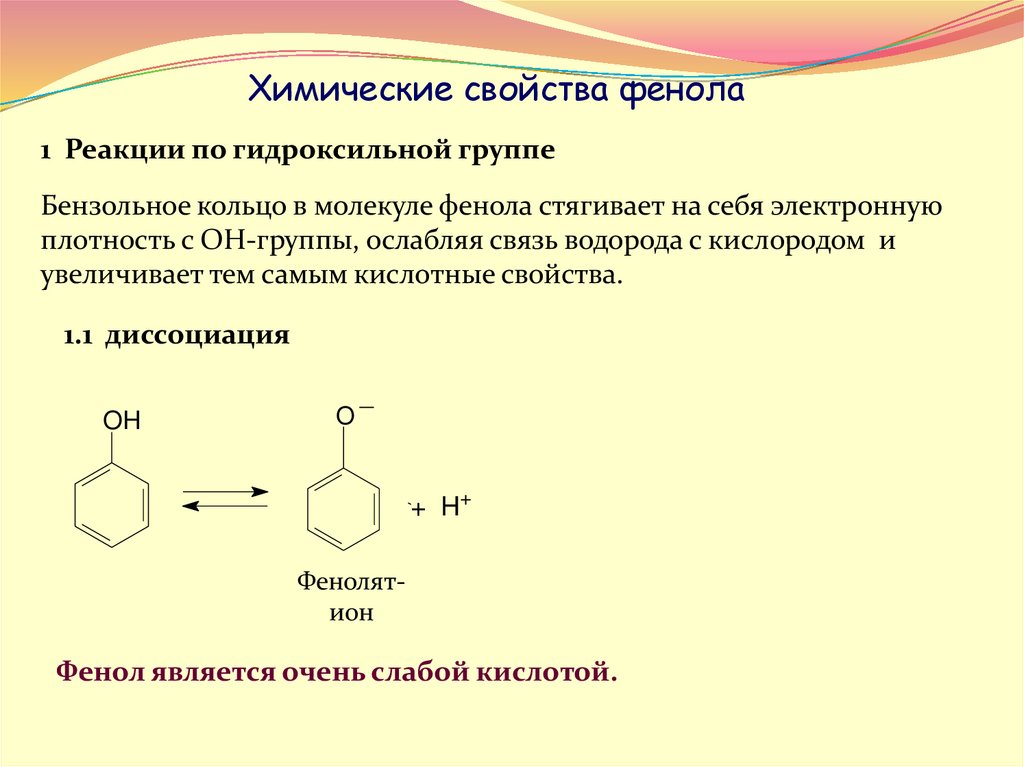
Химические свойства фенола1 Реакции по гидроксильной группе
Бензольное кольцо в молекуле фенола стягивает на себя электронную
плотность с ОН-группы, ослабляя связь водорода с кислородом и
увеличивает тем самым кислотные свойства.
1.1 диссоциация
OH
O
_
+ H+
Фенолятион
Фенол является очень слабой кислотой.
14.
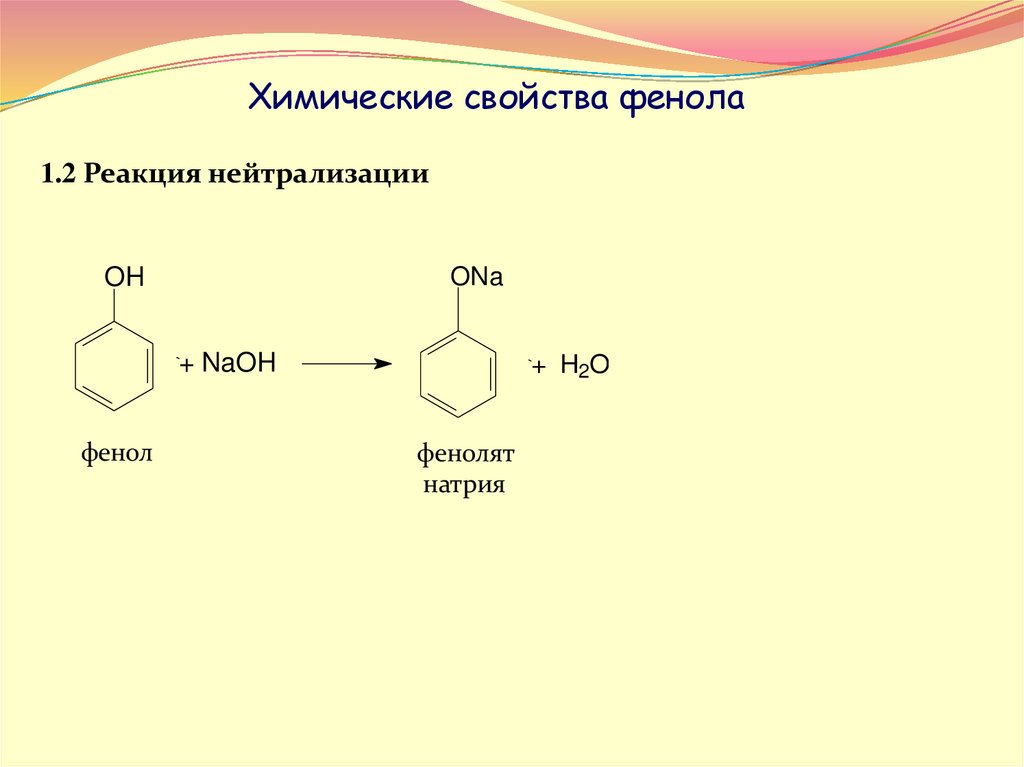
Химические свойства фенола1.2 Реакция нейтрализации
ONa
OH
+ NaOH
фенол
+ H2O
фенолят
натрия
15.
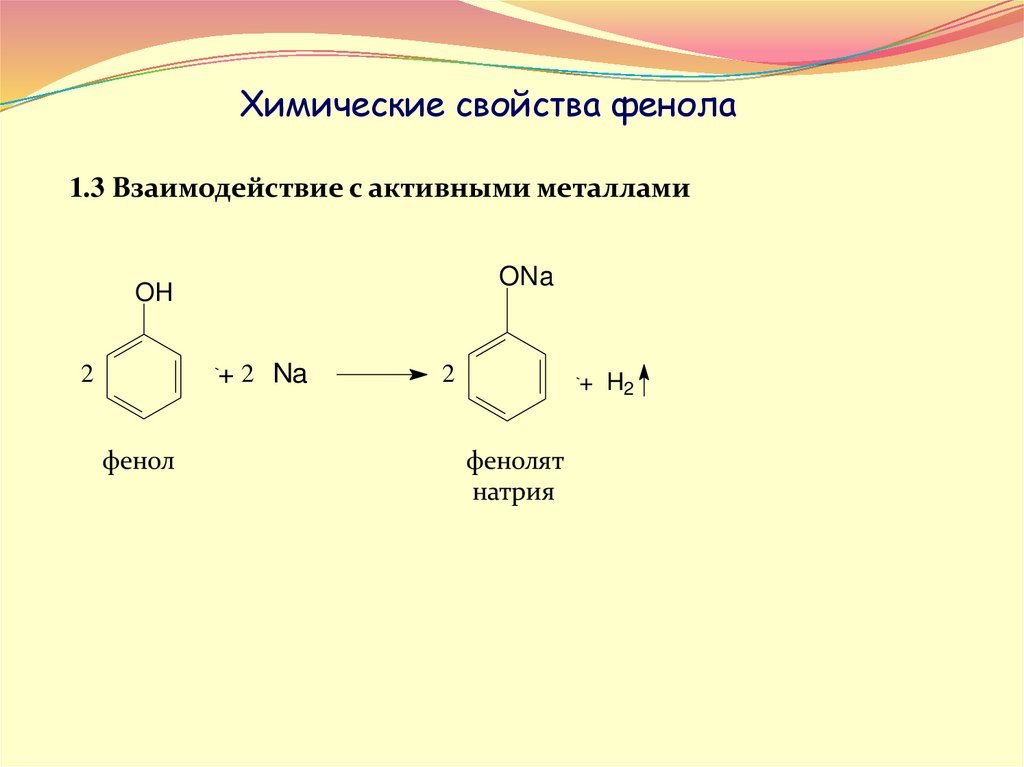
Химические свойства фенола1.3 Взаимодействие с активными металлами
ONa
OH
+ 2 Na
2
фенол
2
+ H2
фенолят
натрия
16.
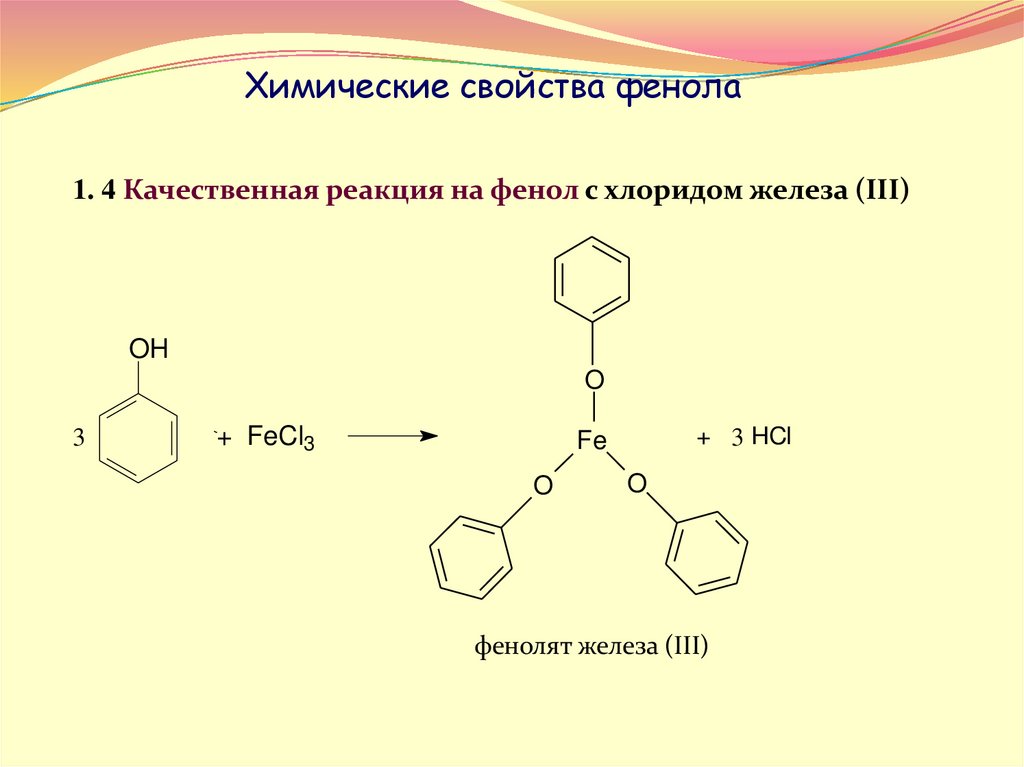
Химические свойства фенола1. 4 Качественная реакция на фенол с хлоридом железа (III)
OH
O
3
+ FeCl3
+ 3 HCl
Fe
O
O
фенолят железа (III)
17.
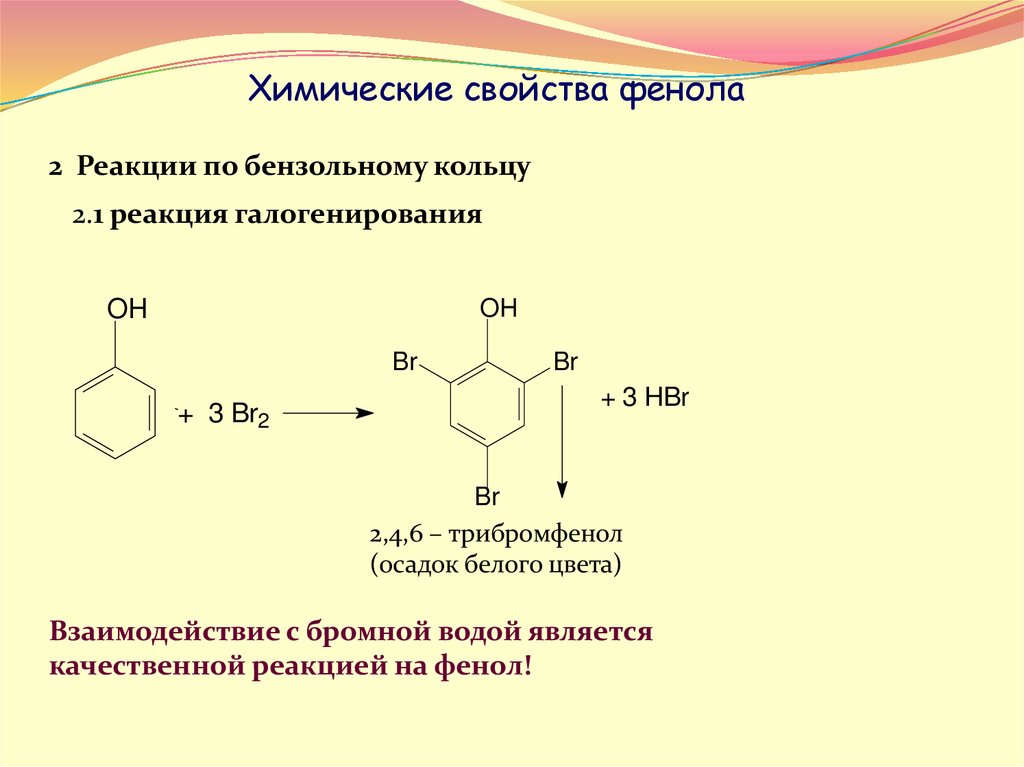
Химические свойства фенола2 Реакции по бензольному кольцу
2.1 реакция галогенирования
OH
OH
Br
+ 3 Br2
Br
+ 3 HBr
Br
2,4,6 – трибромфенол
(осадок белого цвета)
Взаимодействие с бромной водой является
качественной реакцией на фенол!
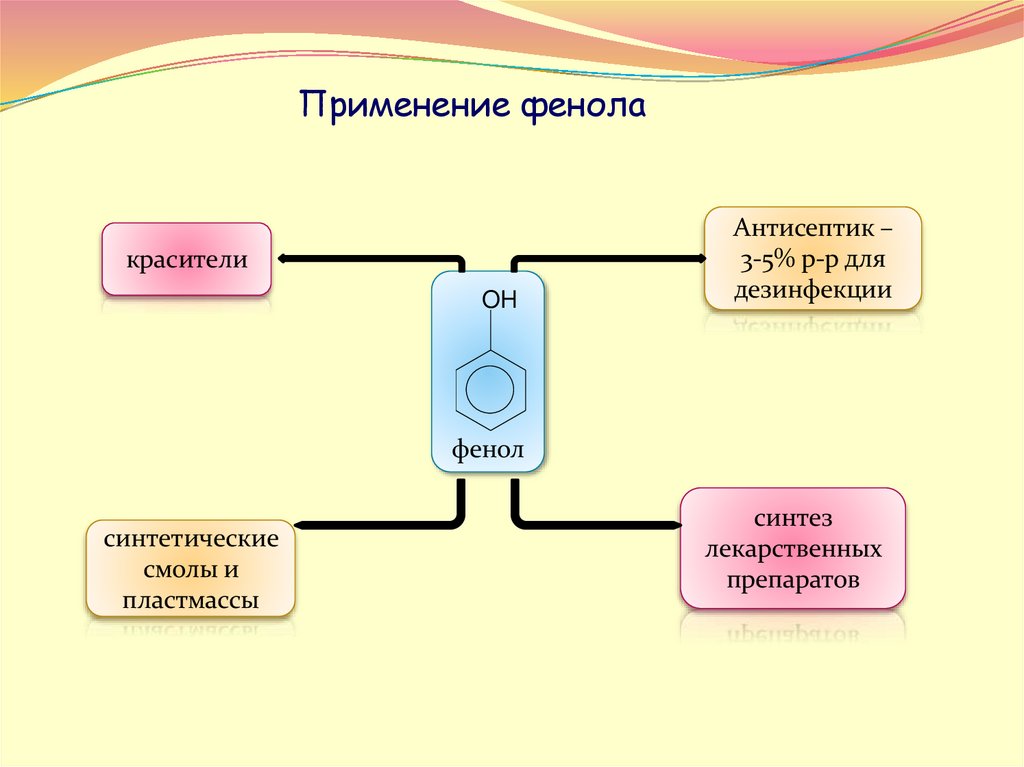
18.
Применение фенолакрасители
OH
Антисептик –
3-5% р-р для
дезинфекции
фенол
синтетические
смолы и
пластмассы
синтез
лекарственных
препаратов
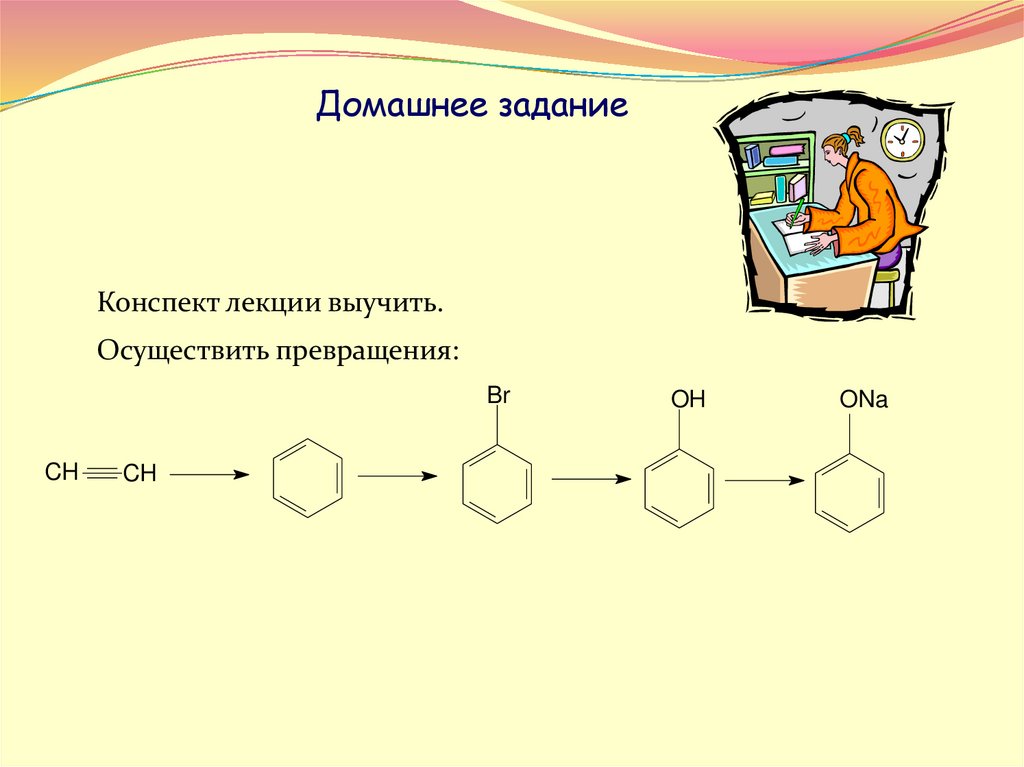
19.
Домашнее заданиеКонспект лекции выучить.
Осуществить превращения:
Br
CH
CH
OH
ONa



 Химия
Химия








