Похожие презентации:
Спирты & Фенолы
1.
Спирты & Фенолы• Классификацмя спиртов и фенолов.
• Электронное строение спиртов и фенолов.
• Химические свойства одноатомных спиртов и
фенолов.
Химические свойства многоатомных спиртов
2.
R-OHСпирты
Aлифатические
Aроматические
насыщенные ненасыщенные
Одноатомные
10 20 30
Многоатомные
3.
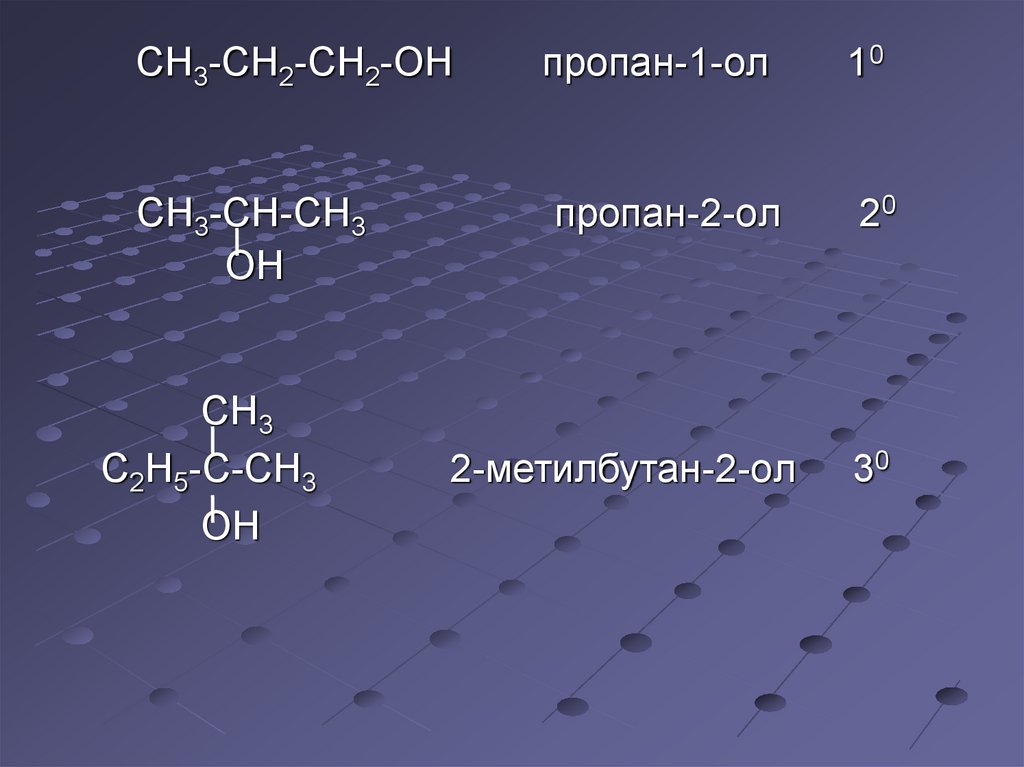
CH3-CH2-CH2-OHCH3-CH-CH3
OH
CH3
C2H5-C-CH3
OH
пропан-1-oл
пропан-2-oл
2-метилбутан-2-oл
10
20
30
4.
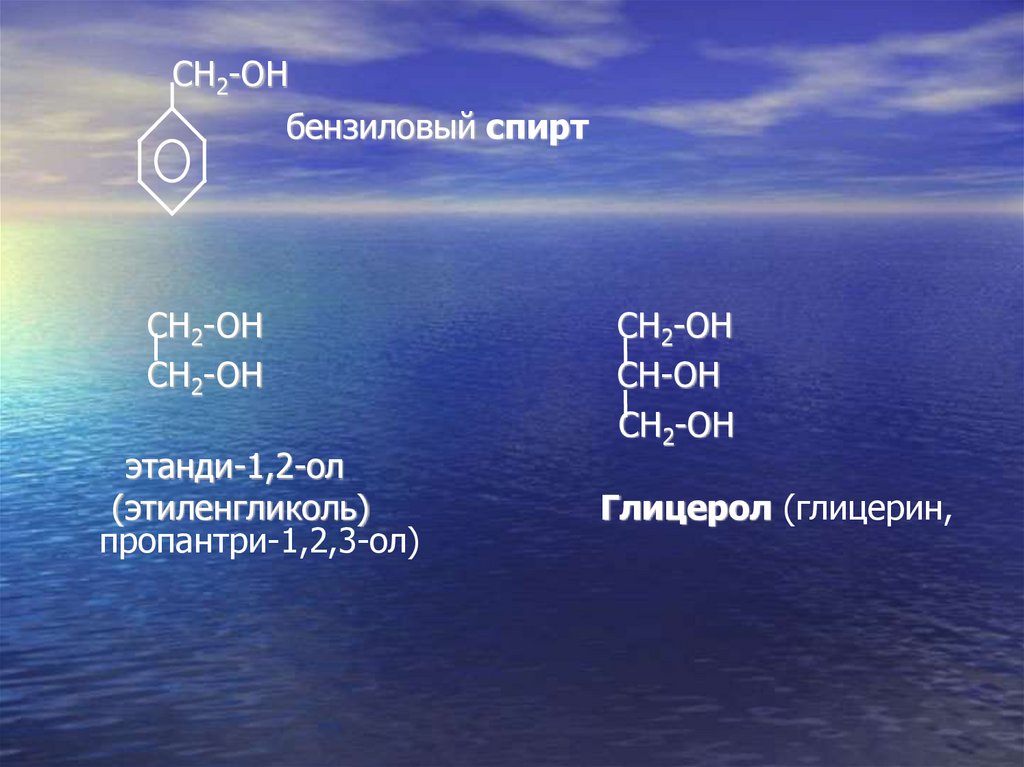
CH2-OHбензиловый спирт
CH2-OH
CH2-OH
этанди-1,2-oл
(этиленгликоль)
пропантри-1,2,3-ол)
CH2-OH
CH-OH
CH2-OH
Глицерол (глицерин,
5.
ФенолыOH
OH
OH
OH
OH
Фенол
Катехол
Гидроквинон
6.
Электронные эффекты в молекулахспиртов
.. δ-
CH3→CH2→CH2→ O ←Hδ+
̈
+I
-I
R-OH ↔ R-O- + H+
Aлкоголят-ион
7.
Индуктивный эффектR +I
R→OH
+I
R→CH←R
+I
OH
+I
10 > 20 > 30
R→C←R
+I
OH
+I
8.
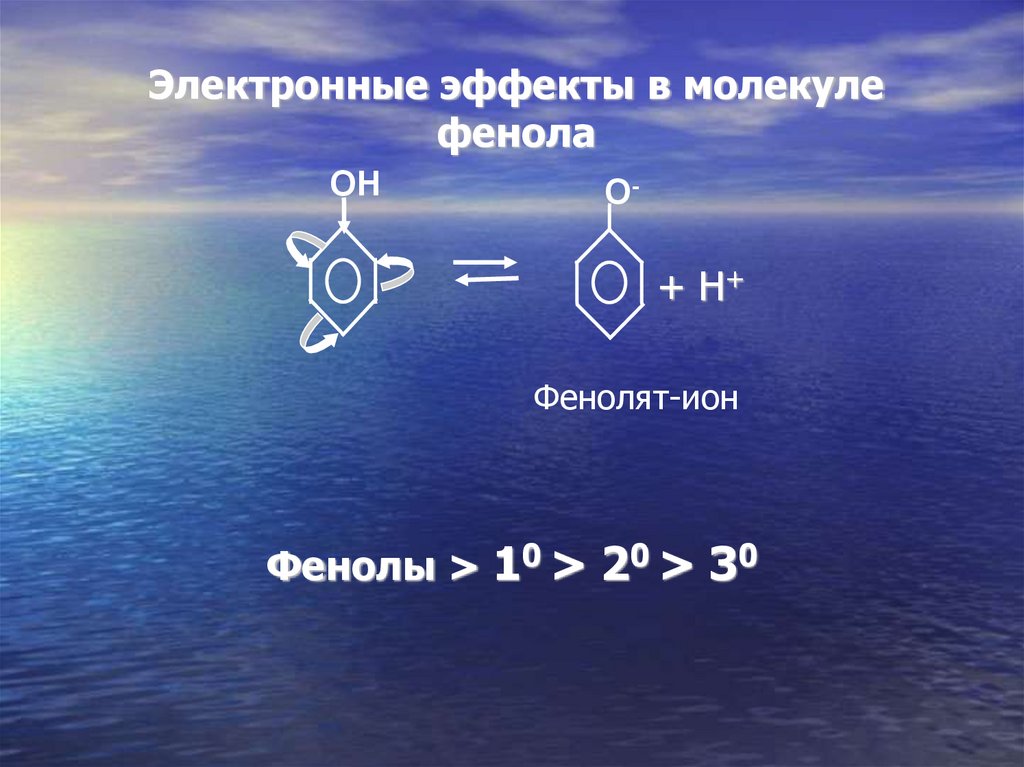
Электронные эффекты в молекулефенола
OH
O-
+ H+
Фенолят-ион
Фенолы > 10 > 20 > 30
9.
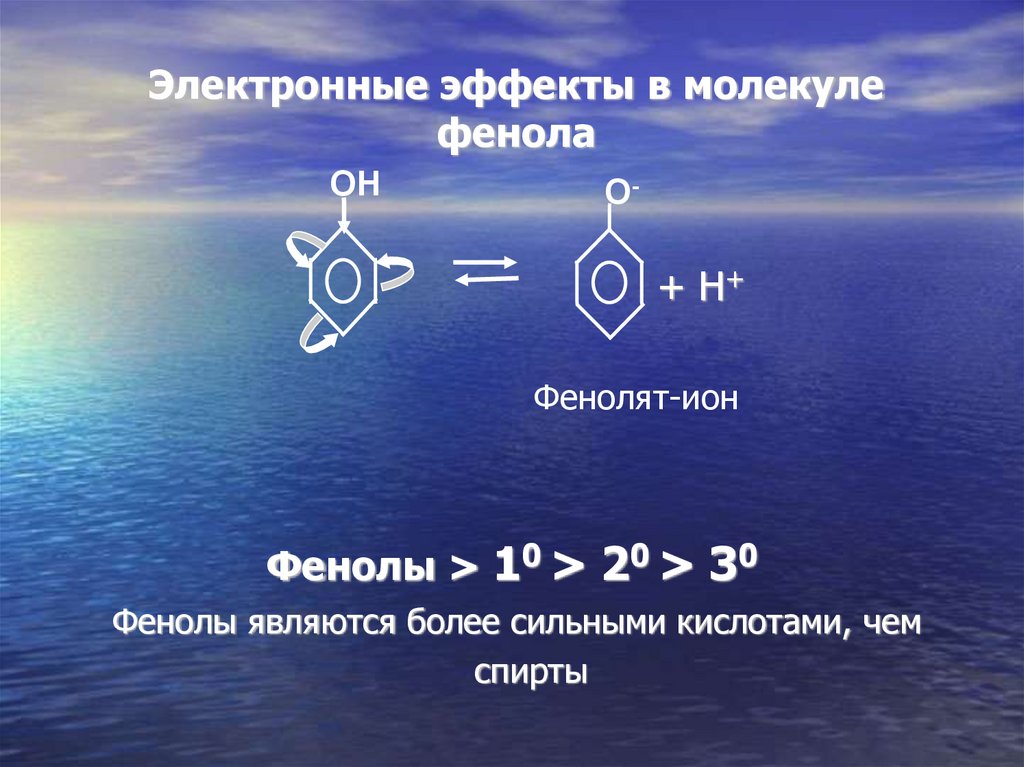
Электронные эффекты в молекулефенола
OH
O-
+ H+
Фенолят-ион
Фенолы > 10 > 20 > 30
Фенолы являются более сильными кислотами, чем
спирты
10.
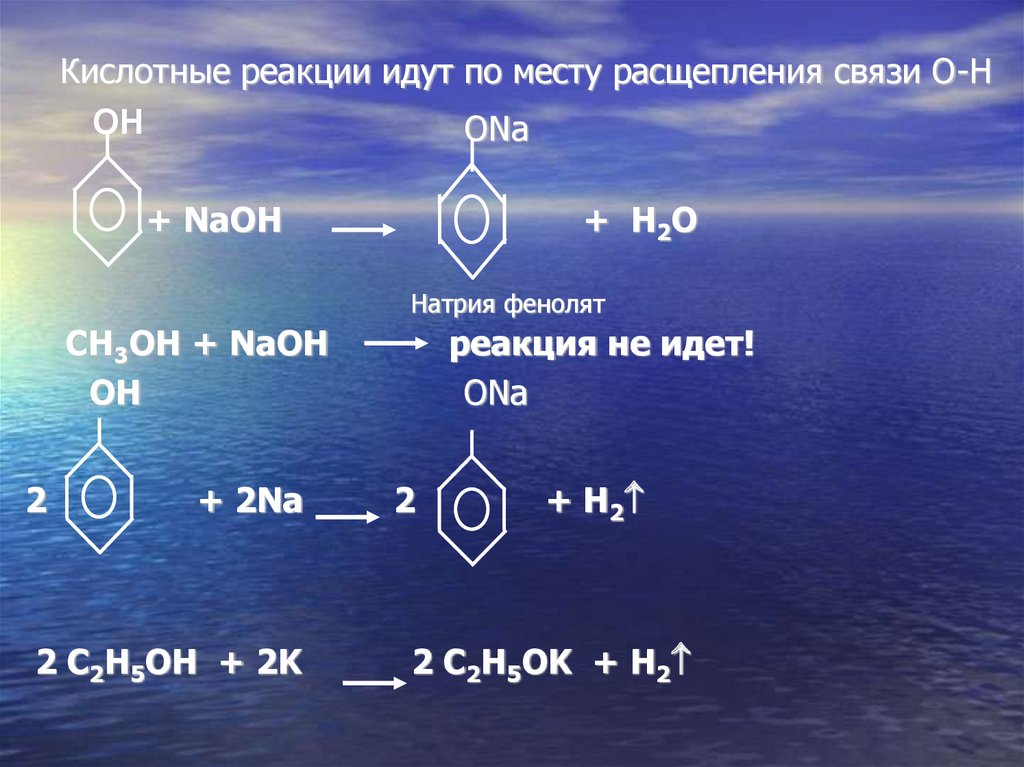
Кислотные реакции идут по месту расщепления связи О-НOH
ONa
+ NaOH
+ H 2O
Натрия фенолят
CH3OH + NaOH
OH
2
+ 2Na
2 C2H5OH + 2K
реакция не идет!
ONa
2
+ H 2
2 C2H5OK + H2
11.
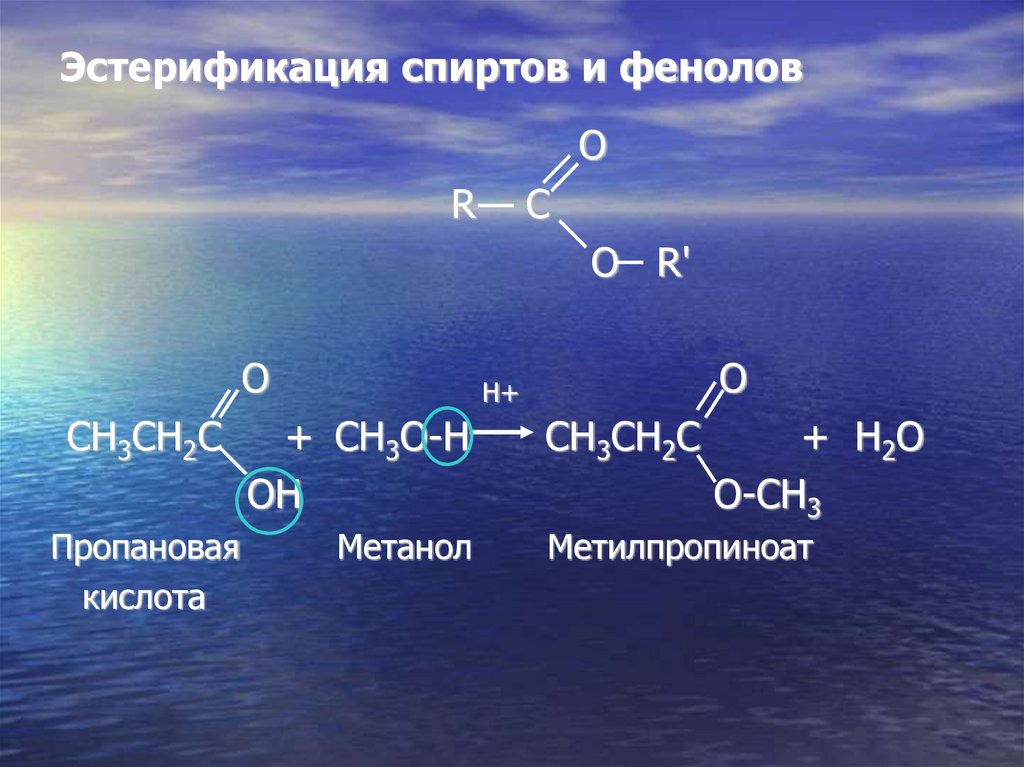
Эстерификация спиртов и феноловO
R
C
O R'
O
CH3CH2C
Пропановая
кислота
O
H+
+ CH3O-H
OH
Meтанол
CH3CH2C
+ H2O
O-CH3
Meтилпропиноат
12.
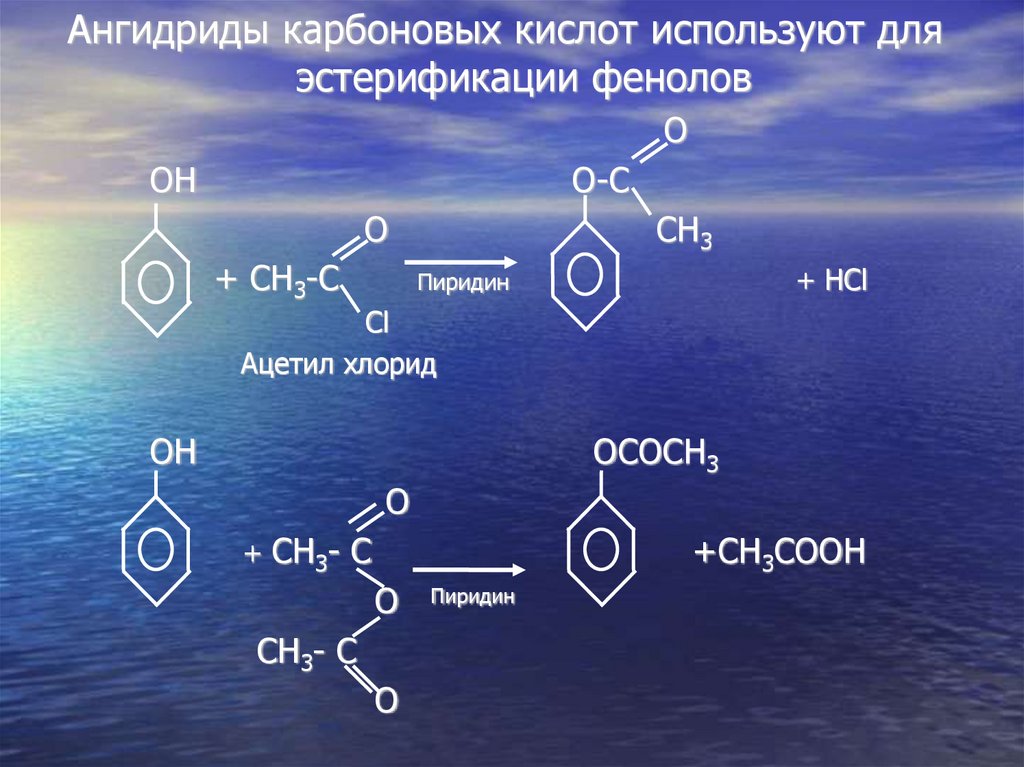
Ангидриды карбоновых кислот используют дляэстерификации фенолов
O
OH
O-C
O
+ CH3-C
CH3
+ HCl
Пиридин
Cl
Ацетил хлорид
OH
OCOCH3
O
+ CH3- C
+CH3COOH
O
CH3- C
O
Пиридин
13.
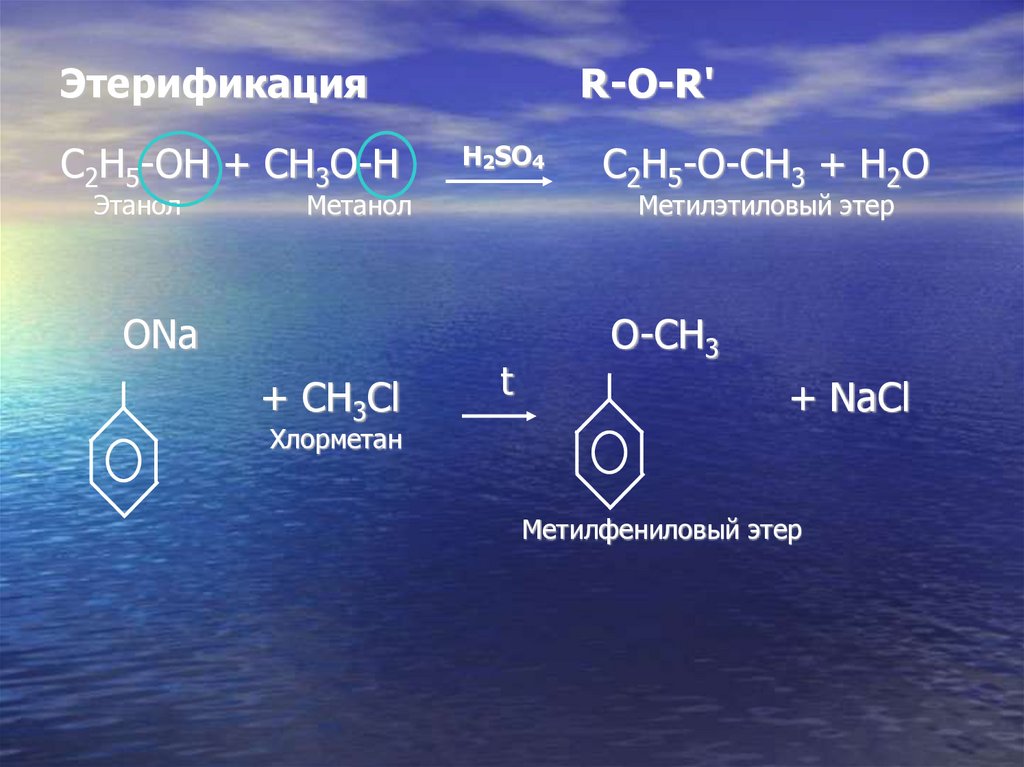
ЭтерификацияC2H5-OH + CH3O-H
Этанол
R-O-R'
H2SO4
Meтанол
ONa
+ CH3Cl
C2H5-O-CH3 + H2O
Метилэтиловый этер
t
O-CH3
+ NaCl
Хлорметан
Метилфениловый этер
14.
SN реакции+
R – OH + HCl
H + R–O
Cl
H
Алкоксония хлорид
H+
1.
R-OH + H+
R-O
H
H+
2.
R- O
R+ + H2O
H
3.
R+ + Cl-
R-Cl
R – Cl + H2O
15.
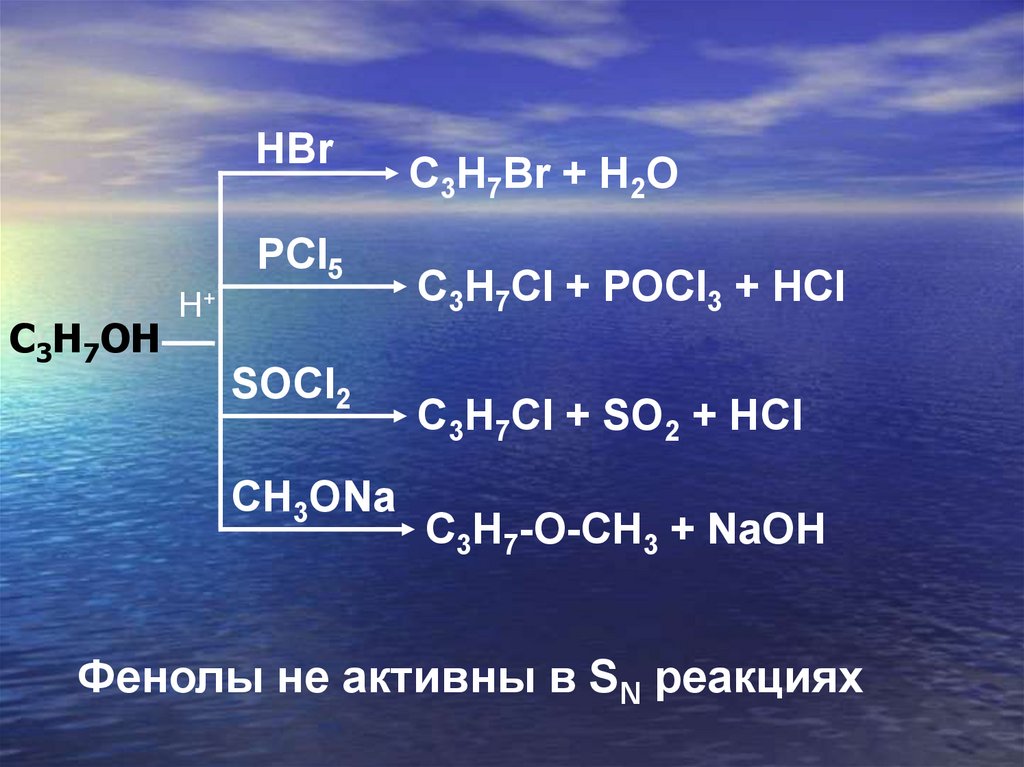
HBrPCl5
C3H7OH
H+
SOCl2
CH3ONa
C3H7Br + H2O
C3H7Cl + POCl3 + HCl
C3H7Cl + SO2 + HCl
C3H7-O-CH3 + NaOH
Фенолы не активны в SN реакциях
16.
α-β элиминирование спиртовβ
α
CH3- CH – CH2-OH
H
CH3- CH=CH2 + H2O
H+, t
Пропен
По правилу Зайцева атом H отщепляется от менее
насыщенного атома C
CH3 β
CH3- C ̶ CH - CH3
OH H
β
H+, t
CH3
CH3- C = CH - CH3 + H2O
1
2
3
2-метилбут-2-eн
4
17.
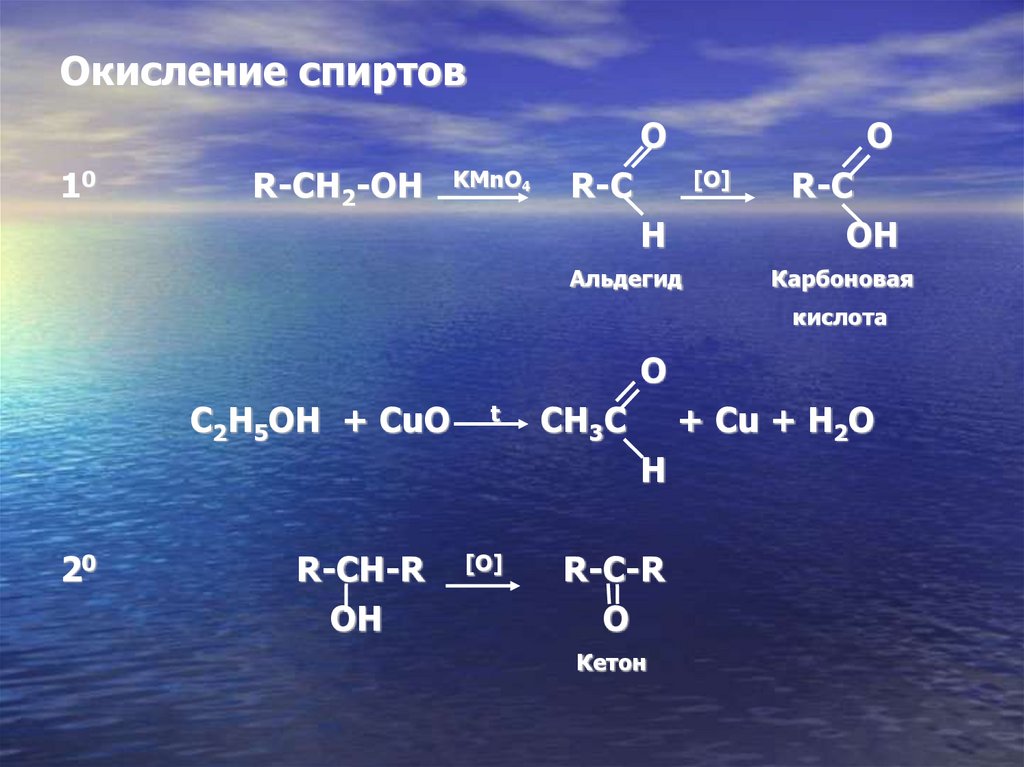
Oкисление спиртовO
10
R-CH2-OH
KMnO4
O
R-C
[O]
H
Aльдегид
R-C
OH
Карбоновая
кислота
O
C2H5OH + CuO
t
CH3C
+ Cu + H2O
H
20
R-CH-R
OH
[O]
R-C-R
O
Кетон
18.
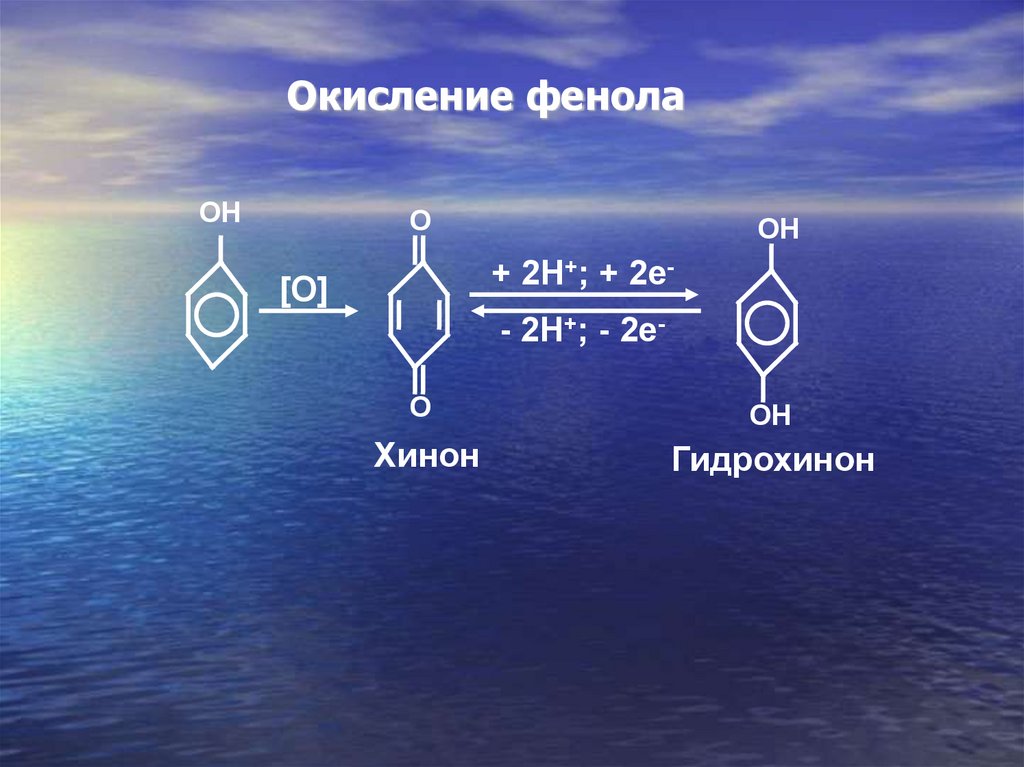
Oкисление фенолаOH
O
OH
+ 2H+; + 2e-
[O]
- 2H+; - 2eO
OH
Хинон
Гидрохинон
19.
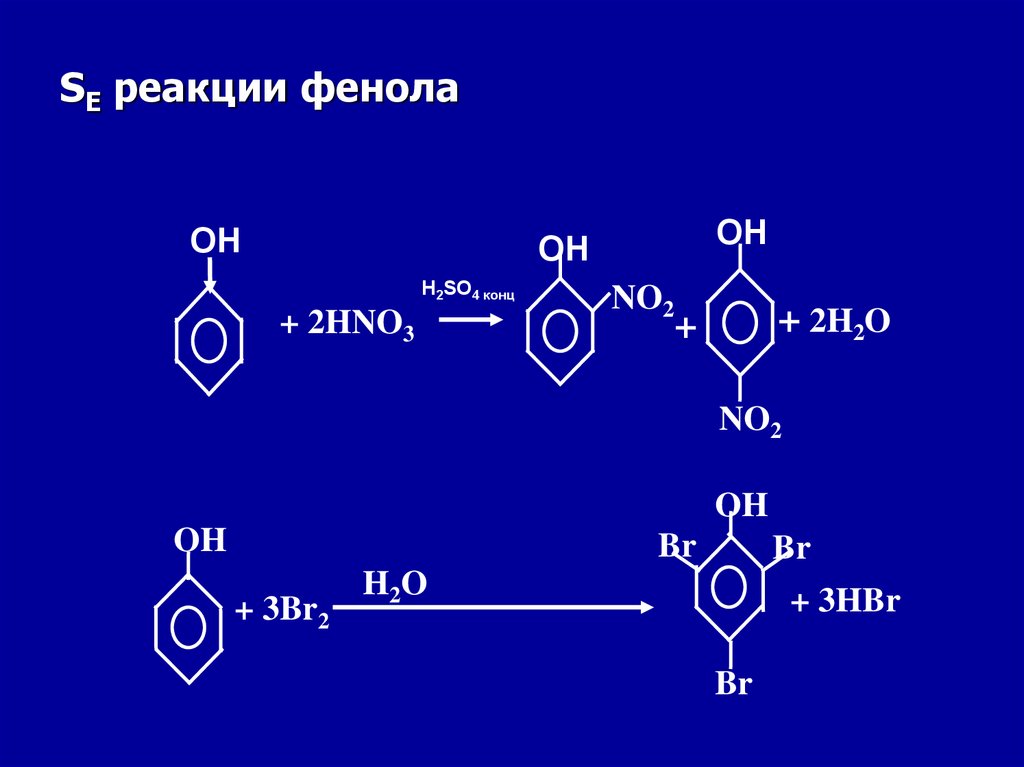
SE реакции фенолаOH
OH
OH
H2SO4 конц
+ 2HNO3
NO2
+ 2H2O
+
NO2
OH
OH
Br
+ 3Br2
Br
H2O
+ 3HBr
Br
20.
Свойства многоатомных спиртов1.
CH2-OH
CH –OH + 3NaOH
CH2-OH
CH2-ONa
CH-ONa + 3H2O
CH2-ONa
Натрия глицерат
2. Эстерификация:
a) с неорганическими кислотами
CH2-OH
CH2-ONO2
CH-OH + 3HNO3 H SO
CH-ONO2 +3H2O
CH2-OH
CH2-ONO2
2
4 конц.
Тринитроглицерол
21.
α CH2-OHβ CH-OH + 2H3PO4
α CH2-OH
CH2-OH
CH2-OH
+ CH-O-PO3H2
-2H O CH-OH
CH2-O-PO3H2
CH2-OH
αβглицеролфосфат
75%
25%
2
b) с жирными кислотами
CH2-OH
CH-OH + 3C17H35COOH
CH2-OH
Стеариновая
кислота
CH2-OCOC17H35
CH-OCOC17H35 + 3H2O
CH2-OCOC17H35
Tристеарин
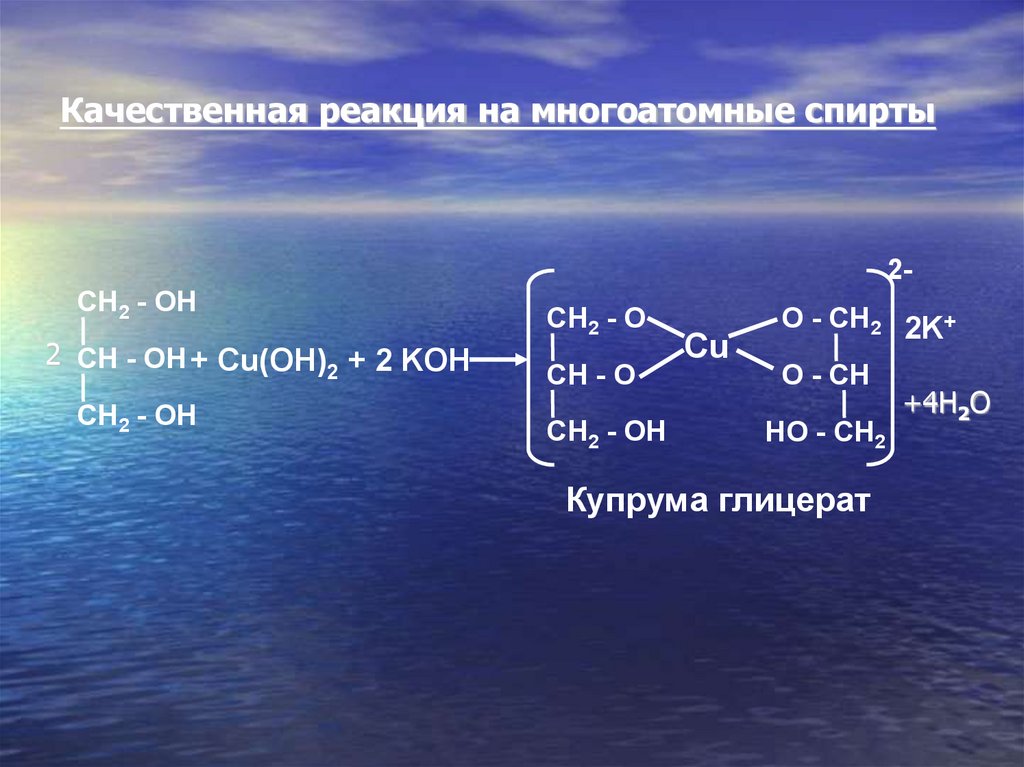
22.
Качественная реакция на многоатомные спирты2CH2 - OH
2 CH - OH + Cu(OH)2 + 2 KOH
CH2 - OH
CH2 - O
CH - O
CH2 - OH
Cu
O - CH2 2K+
O - CH
HO - CH2
Купрума глицерат
+4H2O
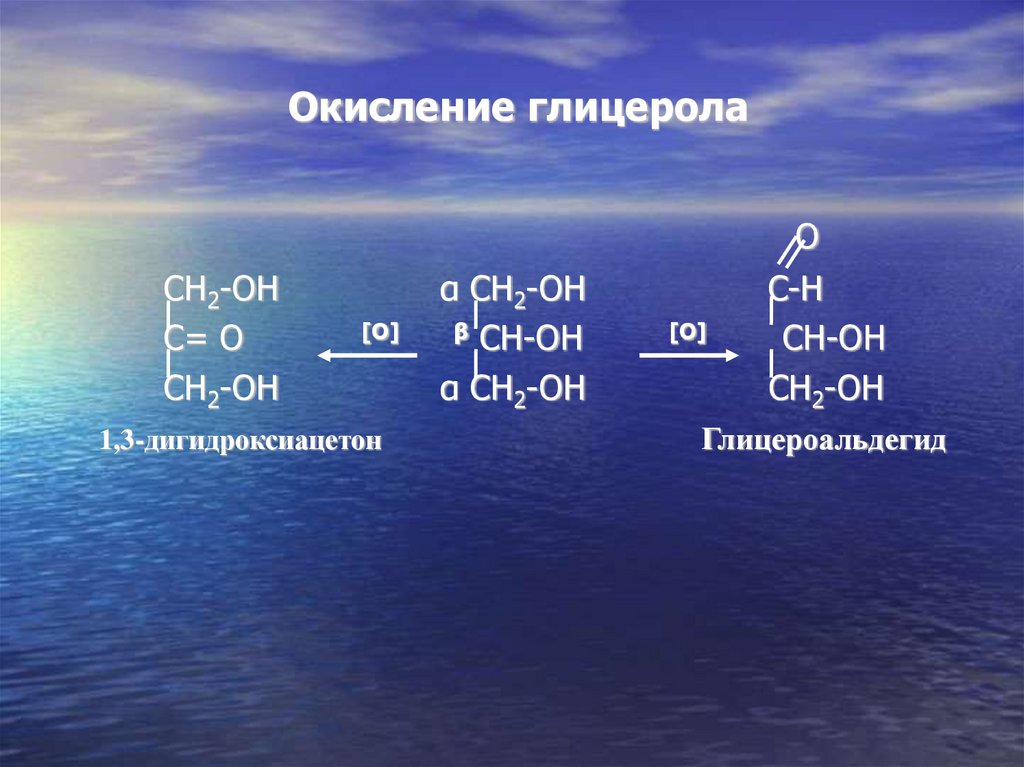
23.
Oкисление глицеролаO
CH2-OH
C= O
CH2-OH
[O]
1,3-дигидроксиацетон
α CH2-OH
β CH-OH
α CH2-OH
[O]
C-H
CH-OH
CH2-OH
Глицероальдегид










 Химия
Химия








