Похожие презентации:
Молекулярная физика
1.
МОЛЕКУЛЯРНАЯ ФИЗИКАПреподаватель: Бахмат С.А.
2.
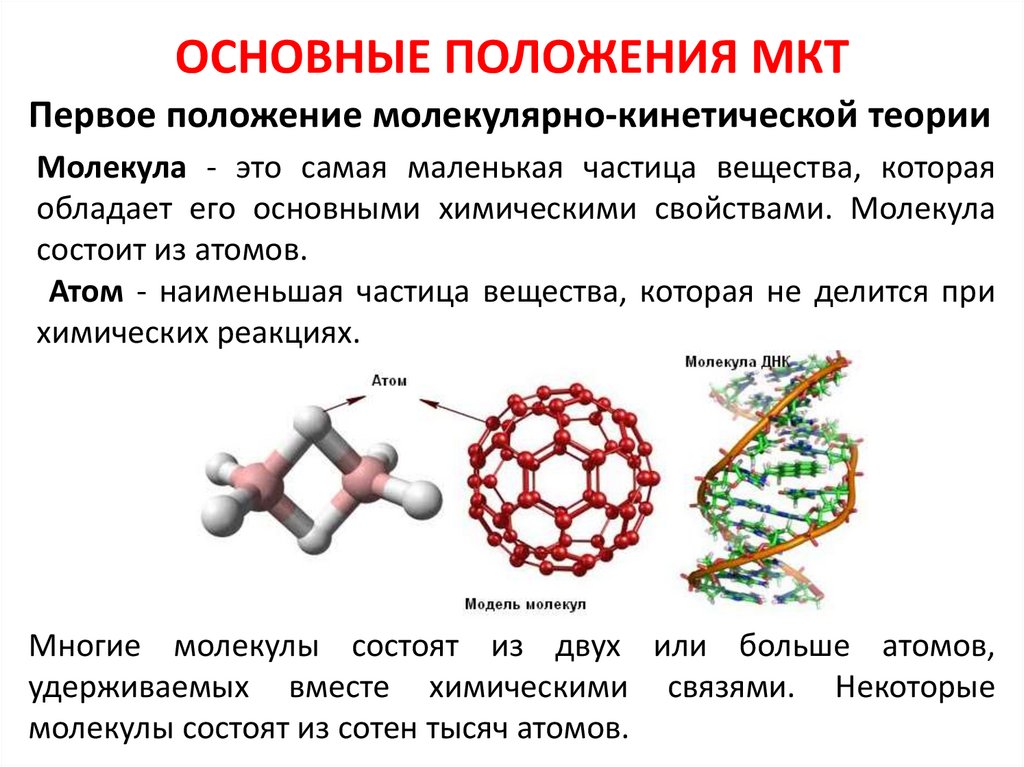
ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТПервое положение молекулярно-кинетической теории
Молекула - это самая маленькая частица вещества, которая
обладает его основными химическими свойствами. Молекула
состоит из атомов.
Атом - наименьшая частица вещества, которая не делится при
химических реакциях.
Многие молекулы состоят из двух или больше атомов,
удерживаемых вместе химическими связями. Некоторые
молекулы состоят из сотен тысяч атомов.
3.
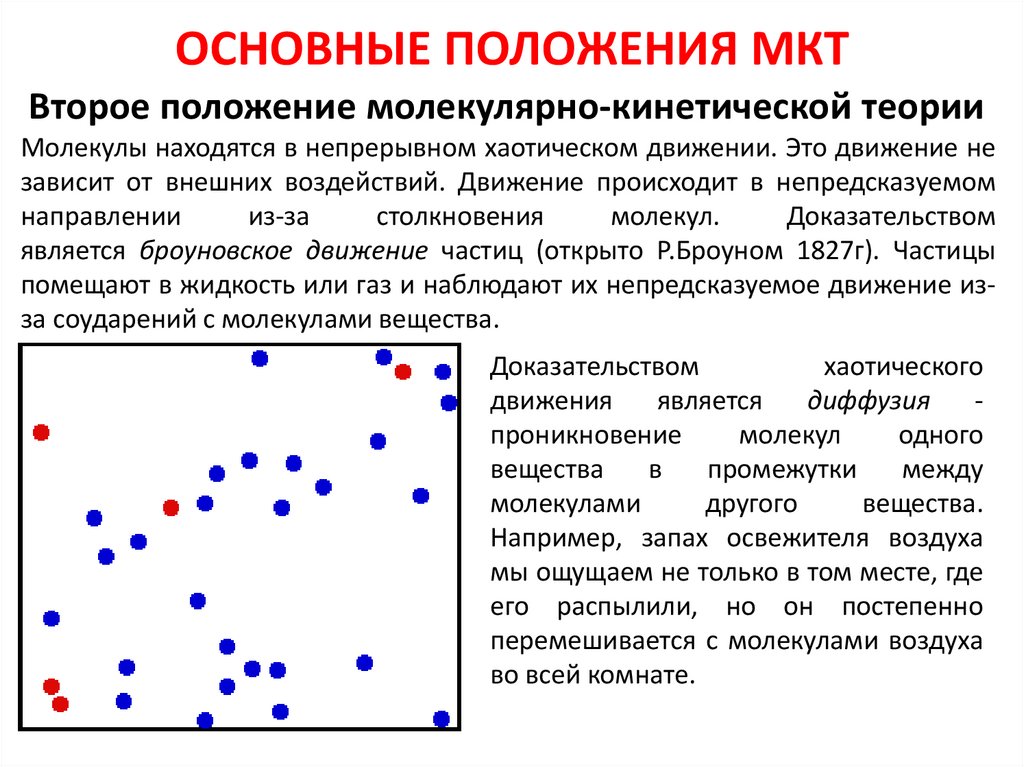
ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТВторое положение молекулярно-кинетической теории
Молекулы находятся в непрерывном хаотическом движении. Это движение не
зависит от внешних воздействий. Движение происходит в непредсказуемом
направлении
из-за
столкновения
молекул.
Доказательством
является броуновское движение частиц (открыто Р.Броуном 1827г). Частицы
помещают в жидкость или газ и наблюдают их непредсказуемое движение изза соударений с молекулами вещества.
Доказательством
хаотического
движения
является
диффузия
проникновение
молекул
одного
вещества
в
промежутки
между
молекулами
другого
вещества.
Например, запах освежителя воздуха
мы ощущаем не только в том месте, где
его распылили, но он постепенно
перемешивается с молекулами воздуха
во всей комнате.
4.
ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТАгрегатное состояние вещества
В газах среднее расстояние между молекулами в
сотни раз превышает их размеры. В основном
молекулы движутся поступательно и равномерно.
После столкновений начинают вращаться.
В жидкостях расстояние между молекулами значительно
меньше. Молекулы совершают колебательное и
поступательное движения. Молекулы через малые
промежутки времени скачкообразно переходят в новые
положения равновесия (мы наблюдаем текучесть
жидкости).
В твердых телах молекулы колеблются и очень редко
перемещаются (только при увеличении температуры).
5.
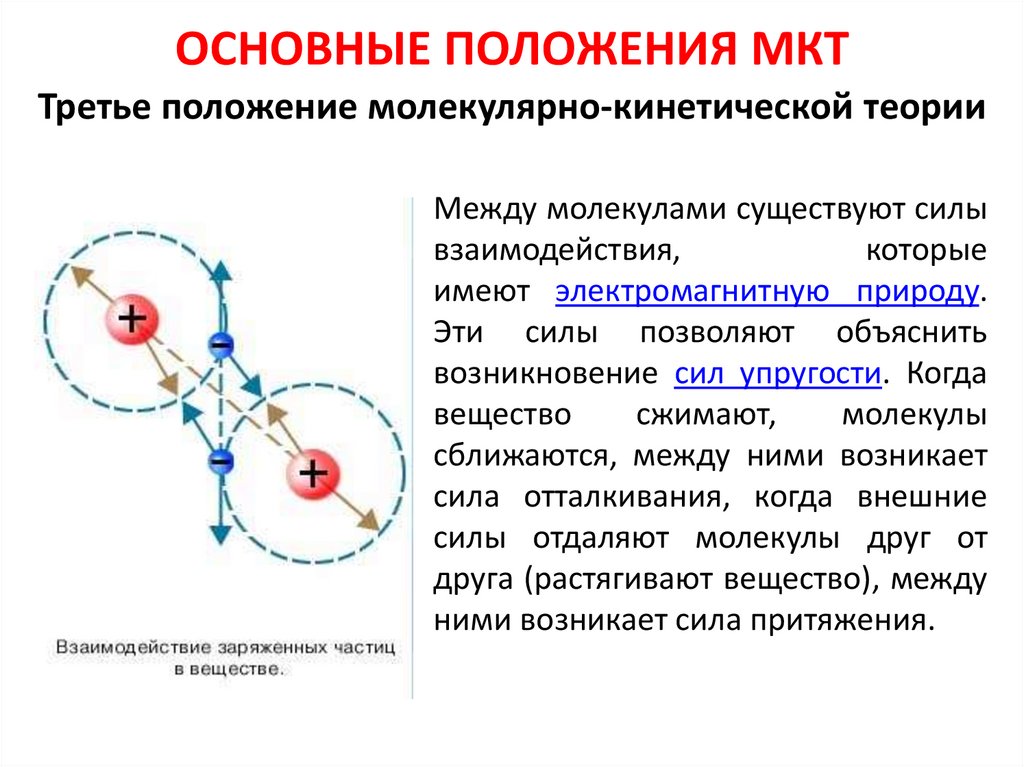
ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТТретье положение молекулярно-кинетической теории
Между молекулами существуют силы
взаимодействия,
которые
имеют электромагнитную природу.
Эти силы позволяют объяснить
возникновение сил упругости. Когда
вещество
сжимают,
молекулы
сближаются, между ними возникает
сила отталкивания, когда внешние
силы отдаляют молекулы друг от
друга (растягивают вещество), между
ними возникает сила притяжения.
6.
ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТПлотность вещества
Это скалярная величина, которая определяется по
формуле
Плотность веществ - известные табличные значения
7.
ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТХимические характеристики вещества
Постоянная Авогадро NA - число атомов, содержащихся в 12г
изотопа углерода
Количество вещества - это отношение числа элементов этого
вещества к постоянной Авогадро
1 моль любого вещества содержит одинаковое число частиц, это
число равно постоянной Авогадро.
8.
ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТХимические характеристики вещества
Молярная масса M - это масса одного моля вещества
Если тело состоит из N молекул массой m0, то масса тела
9.
ОСНОВНЫЕ ПОЛОЖЕНИЯ МКТХимические характеристики вещества
Концентрация частиц - это количество частиц в объеме
Можно вывести формулы
10.
Идеальный газЭто несуществующая физическая модель газа,
который состоит из большого числа молекул,
размеры которых ничтожно малы по сравнению
со средними расстояниями между ними.
Молекулы
такого
газа
можно
считать материальными точками, это означает,
что их вращательное и колебательное движения
не принимаются во внимание. Движение
молекул происходит без столкновений с
другими молекулами, подчиняется законам
Ньютона. Соударения молекул со стенками
сосуда являются абсолютно упругими.
11.
Параметры состояния газаДавление, температура и объем - параметры состояния
газа. Или их называют макропараметрами.
Температура - внешняя характеристика скоростей частиц
газа.
Давление - внешняя характеристика соударений со
стенками, например, сосуда.
Объем - место, куда заключены частицы газа. Газ занимает
весь предоставленный ему объем. Существуют еще внешние
параметры, например тела или поля, действующие на газ из вне.
Микропараметры (маленькие, внутренние характеристики)
газа - это параметры, которые мы не можем оценить без
специальных экспериментов, например, скорость и направление
движения каждой молекулы газа.
Состояние термодинамической системы, когда все ее
параметры при неизменных внешних условиях не изменяются со
временем, называют равновесным.
12.
ДавлениеЭто физическая скалярная
определяется по формуле
величина,
которая
13.
Атмосферное давлениеАтмосфера - это воздушная оболочка Земли, которая
удерживается гравитационными силами. Атмосфера имеет вес и
давит на все тела на Земле. Давление атмосферы составляет
около 760 мм.рт.ст. или 1 атм., или 101325Па. Миллиметр
ртутного столба, атмосфера - это различные внесистемные
единицы измерения давления. Атмосферное давление
уменьшается на 1 мм.рт.ст. при поднятии над Землей на каждые
11м.
14.
Атмосферное давлениеЧто такое давление в 1 атм? Рукопожатие крепкого
мужчины составляет 0,1 атм, удар боксера составляет
несколько атмосферных единиц. Давление каблукашпильки составляет 100 атмосфер. Если на ладонь
положить гирю в 100 кг, то получим неравномерное
давление в одну атмосферу, при погружении на 10 м
под воду получим равномерное давление в 1
атмосферу. Равномерное давление легко переносится
человеческим организмом. Нормальное атмосферное
давление, которое действует на каждого человека,
компенсируется внутренним давлением, поэтому его
мы совершенно не замечаем, несмотря на то, что оно
является достаточно существенным.
15.
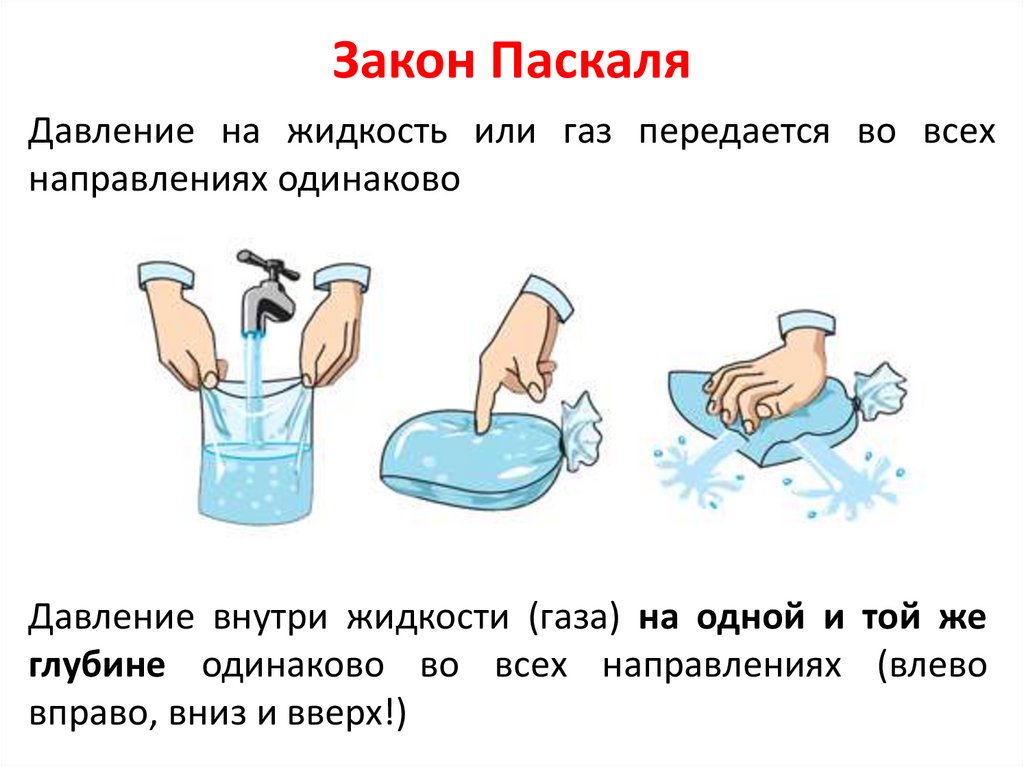
Закон ПаскаляДавление на жидкость или газ передается во всех
направлениях одинаково
Давление внутри жидкости (газа) на одной и той же
глубине одинаково во всех направлениях (влево
вправо, вниз и вверх!)
16.
Гидростатическое давлениеЭто давления столбика жидкости на дно сосуда. Какая сила
создает давление? Жидкость обладает весом, который давит на
дно.
Давление жидкости на дно
17.
Гидростатическое давлениеДавление на дно сосуда не зависит от формы сосуда, но
зависит от площади его дна. При этом сила давления на
дно может быть и больше и меньше силы тяжести
жидкости
в
сосуде.
В
этом
заключается "гидростатический парадокс".
На
стенку
сосуда
гидростатическое
давление
распределено неравномерно: у поверхности жидкости оно
равно нулю (без учета атмосферного давления), внутри
жидкости изменяется прямо пропорционально глубине и
на уровне дна достигает значения
.
Это переменное давление можно заменить средним
давлением
18.
Сообщающиеся сосудыЭто сосуды, которые имеют общий канал
внизу.
Однородная жидкость устанавливается в
сообщающихся сосудах на одном уровне
независимо от формы сосудов, как видно
на фотографии.
Разнородные жидкости устанавливаются в
сообщающихся сосудах согласно формуле
19.
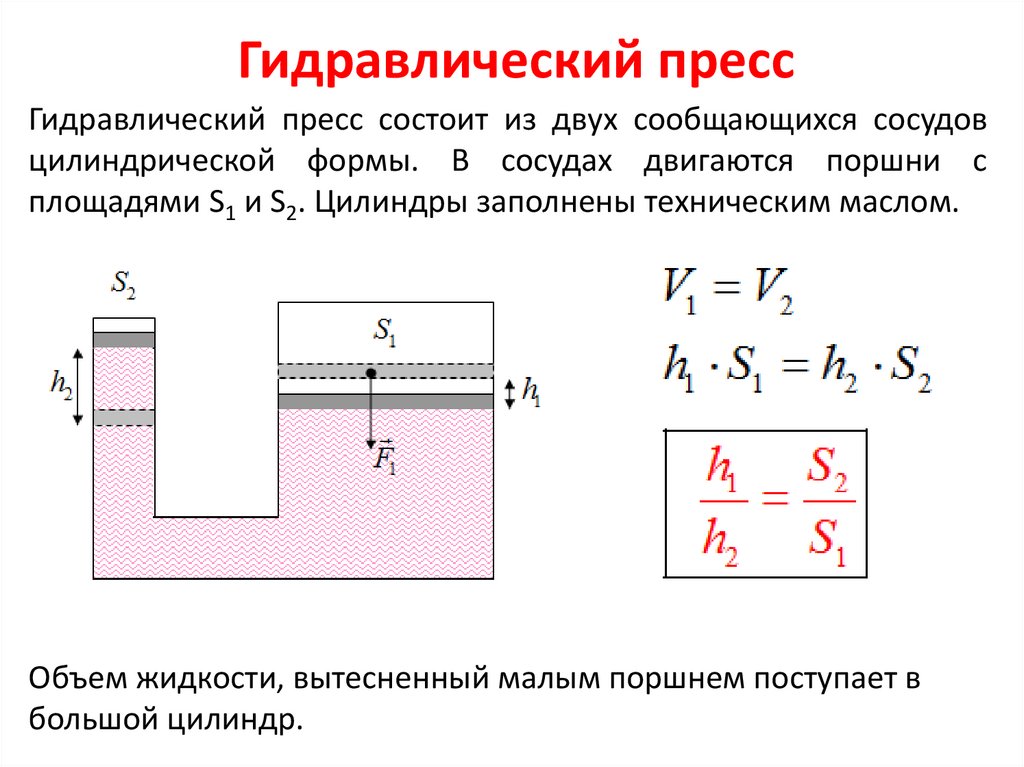
Гидравлический прессГидравлический пресс состоит из двух сообщающихся сосудов
цилиндрической формы. В сосудах двигаются поршни с
площадями S1 и S2. Цилиндры заполнены техническим маслом.
Объем жидкости, вытесненный малым поршнем поступает в
большой цилиндр.
20.
Гидравлический прессГидравлический пресс дает выигрыш в силе во столько раз, во
сколько площадь большего поршня больше площади меньшего.
Выигрыша в работе гидравлический пресс не дает.
На практике вследствие наличия трения:
21.
Давление не перпендикулярной кповерхности силы
Если сила направлена под углом к нормали
(перпендикуляру), то давление определяется по
формуле
22.
Практическое применение давленияГазы
и
жидкости,
находящиеся
под
давлением, нашли широкое применение в
промышленной
технике.
Например,
пневматический отбойный молоток. При
помощи сжатого воздуха работают также двери
в автобусах и метро, тормоза поездов и
грузовых автомобилей.
Встречаются также механизмы, работающие
при помощи сжатой жидкости. Они называются
гидравлическими.
Например,
устройство
гидравлического пресса.
23.
Атмосферное давление открытие иизмерение
Численное значение атмосферного давления было определено опытным
путем в 1643 году итальянским ученым Э.Торричелли.
Стеклянную трубку длиной около метра, запаянную с одного конца,
наполняют доверху ртутью. Затем, плотно закрыв отверстие пальцем, трубку
переворачивают и опускают в чашу со ртутью, после чего палец убирают.
Ртуть из трубки начинает выливаться, но не вся: остаётся «столб» » 76 см
высотой, считая от уровня в чаше. Примечательно, что эта высота не зависит
ни от длины трубки, ни от глубины её погружения.
24.
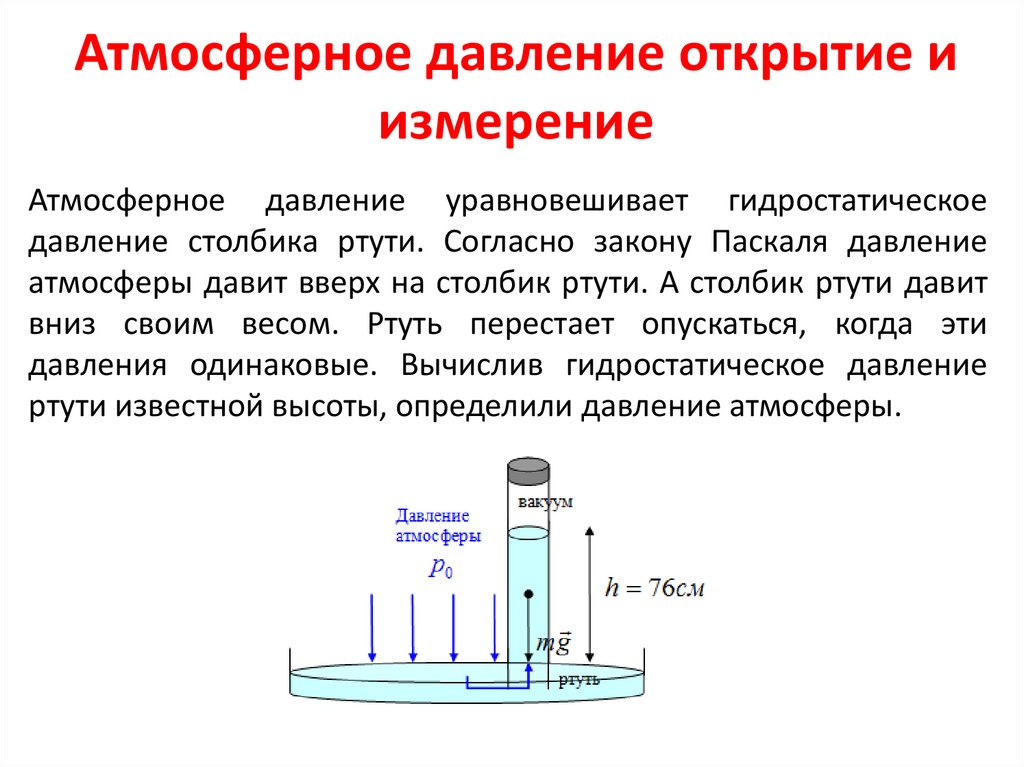
Атмосферное давление открытие иизмерение
Атмосферное давление уравновешивает гидростатическое
давление столбика ртути. Согласно закону Паскаля давление
атмосферы давит вверх на столбик ртути. А столбик ртути давит
вниз своим весом. Ртуть перестает опускаться, когда эти
давления одинаковые. Вычислив гидростатическое давление
ртути известной высоты, определили давление атмосферы.
25.
Атмосферное давление открытие иизмерение
Трубка Торричелли с линейкой является
простейшим барометром – прибором
для измерения атмосферного давления
Для
измерения
атмосферного
давления используют также барометранероид.
Поскольку атмосферное давление
уменьшается по мере удаления от
поверхности Земли, то шкалу анероида
можно проградуировать в метрах. В
этом
случае
он
называется альтиметром.
26.
Возникновение силы АрхимедаПусть прямоугольный металлический брусок площадью основания S и
высотой h лежит на дне сосуда, в который налита вода до высоты H, H>h. Как
определить силу давления бруска на дно сосуда?
Возможны два случая! Пусть брусок неплотно
прилегает ко дну сосуда, тогда снизу на брусок
действует сила давления жидкости. Эта сила
больше силы давления жидкости сверху,
поэтому возникает сила Архимеда. Сила
Архимеда - результат разницы силы
гидростатического давления на нижнюю грань
бруска и верхнюю грань, зависит от высоты
бруска и площади основания.
Используем 2 закон Ньютона:
27.
Возникновение силы АрхимедаРассмотрим второй возможный случай. Пусть брусок прилегает ко дну так
плотно, что жидкость под него не подтекает. Снизу отсутствует давление
жидкости, следовательно сила Архимеда равна нулю. Сверху же на брусок
действует сила давления жидкости и атмосферы.
Используем 2 закон Ньютона для этого
случая:
p0 - атмосферное давление,
p - гидростатическое давление столба
жидкости высотой H-h.
28.
Идеальный газЭто несуществующая физическая модель газа, который
состоит из большого числа молекул, размеры которых
ничтожно малы по сравнению со средними
расстояниями между ними. Молекулы такого газа
можно считать материальными точками, это означает,
что их вращательное и колебательное движения не
принимаются во внимание. Движение молекул
происходит без столкновений с другими молекулами,
подчиняется законам Ньютона. Соударения молекул со
стенками сосуда являются абсолютно упругими.
29.
Параметры состояния газаДавление, температура и объем - параметры состояния газа.
Или их называют макропараметрами. Температура - внешняя
характеристика скоростей частиц газа. Давление - внешняя
характеристика соударений со стенками, например, сосуда.
Объем - место, куда заключены частицы газа. Газ занимает весь
предоставленный ему объем.
Существуют еще внешние параметры, например тела или
поля, действующие на газ из вне.
Микропараметры (маленькие, внутренние характеристики)
газа - это параметры, которые мы не можем оценить без
специальных экспериментов, например, скорость и направление
движения каждой молекулы газа.
Состояние термодинамической системы, когда все ее
параметры при неизменных внешних условиях не изменяются со
временем, называют равновесным.
30.
Основное уравнение молекулярнокинетической теорииУравнение
связывает
микропараметры и макропараметры
(давление, объем и температуру)
идеального газа.
Рассмотрим идеальный газ, который
находится в кубическом сосуде. Каждая
молекула упруго сталкивается со
стенкой сосуда, при этом изменятся ее
импульс. Столкновение всех молекул со
стенкой на макроуровне ощущается как
давление газа на сосуд. В формулах
будут присутствовать средние значения,
потому что какая-то молекула движется
быстрее, какая-то помедленнее, для
того, чтобы оценить примерную
скорость,
будем
брать
средние
значения.
Основное уравнение МКТ имеет вид
31.
Основное уравнение молекулярнокинетической теорииСредний квадрат скорости молекул
32.
Основное уравнение молекулярнокинетической теорииСредняя квадратичная скорость vкв молекул это квадратный
корень из среднего квадрата скорости
Средняя кинетическая энергия молекул
33.
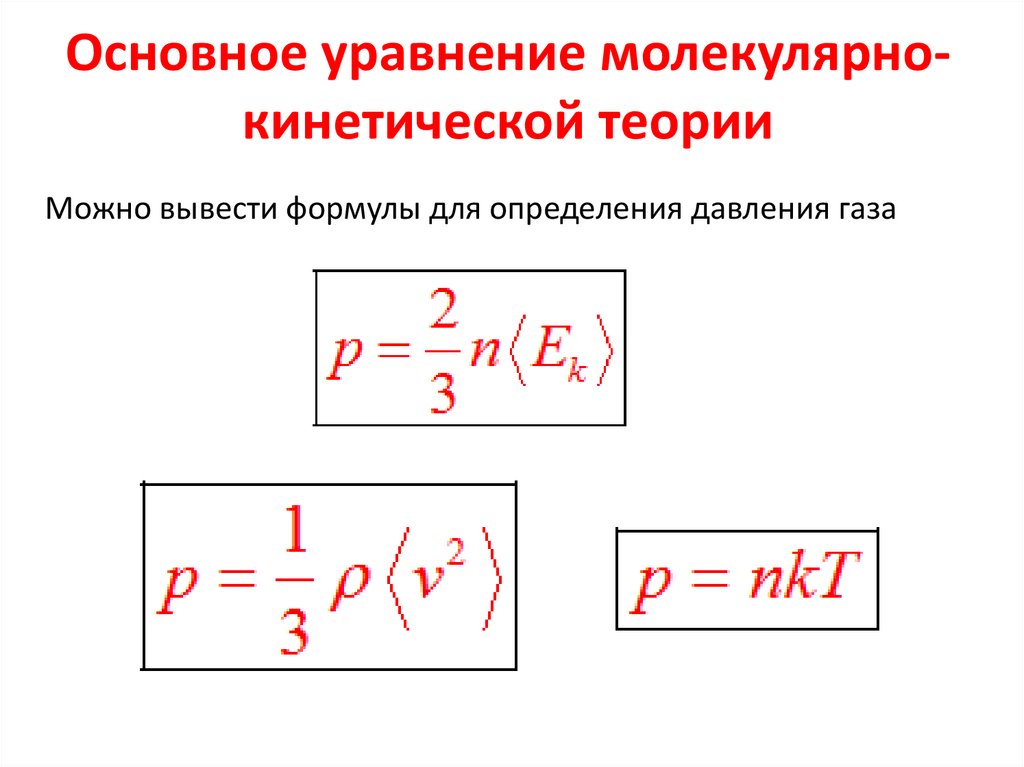
Основное уравнение молекулярнокинетической теорииМожно вывести формулы для определения давления газа
34.
ТемператураТемпература - то макропараметр, который
характеризует способность тел к теплопередаче. Если
два тела разной температуры контактируют, то
произойдет переход энергии или передача теплоты от
более горячего к холодному. Установится тепловое
равновесие, все части будут одинаковой температуры.
35.
ТемператураТемпература характеризует интенсивность движения частиц, поэтому связана
со средней кинетической энергией частиц. Из опыта известно, что средняя
кинетическая энергия молекул не зависит от вида газа и определяется
температурой.
Связь между температурами по шкале
Цельсия и по шкале Кельвина
36.
Уравнение состояния идеального газаВзяли порцию газа некоторой массы и начали
проводить над ней эксперименты. Например, изменяли
некоторый параметр (например, температуру T) и
наблюдали, как изменяются другие два параметра
(объем V и давление p). При увеличении температуры,
молекулы двигаются быстрее, соударения происходят
чаще, значит, давление увеличивается и газ стремится
занять больший объем. Или, если уменьшить объем, то
частицам газа становится тесно, они чаще соударяются,
увеличивается давление, а от большого числа
соударений их скорость может увеличиваться, то есть
может увеличиться температура.
37.
Уравнение состояния идеального газаИнтуитивно пришли к зависимости трех макропараметров газа,
которую вывел французский физик Б. Клапейрон
или
В любом состоянии одной и той же порции газа
величина
остается постоянной.
38.
Уравнение состояния идеального газаД.И. Менделеев исследовал влияние изменения массы газы на
макропараметры. Получил зависимость, которое носит название уравнение
Менделеева-Клапейрона, оно же уравнение состояния идеального газа
Используя формулы химических характеристик вещества,
основное уравнение возможно записать в ином эквивалентном
виде.
39.
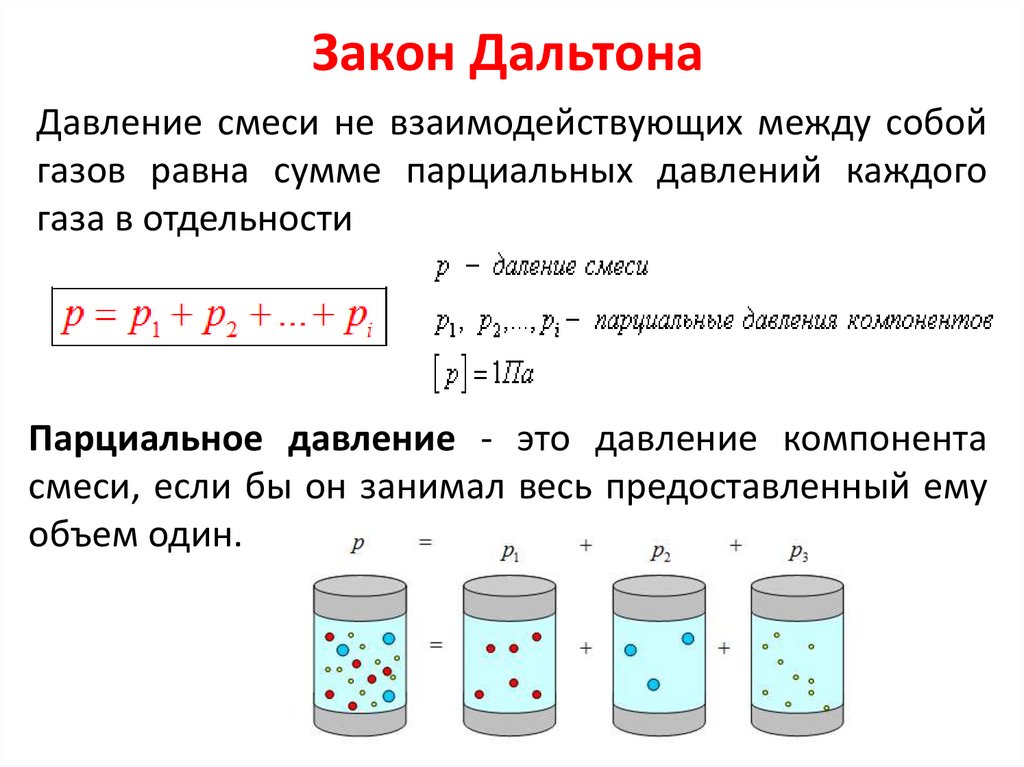
Закон ДальтонаДавление смеси не взаимодействующих между собой
газов равна сумме парциальных давлений каждого
газа в отдельности
Парциальное давление - это давление компонента
смеси, если бы он занимал весь предоставленный ему
объем один.
40.
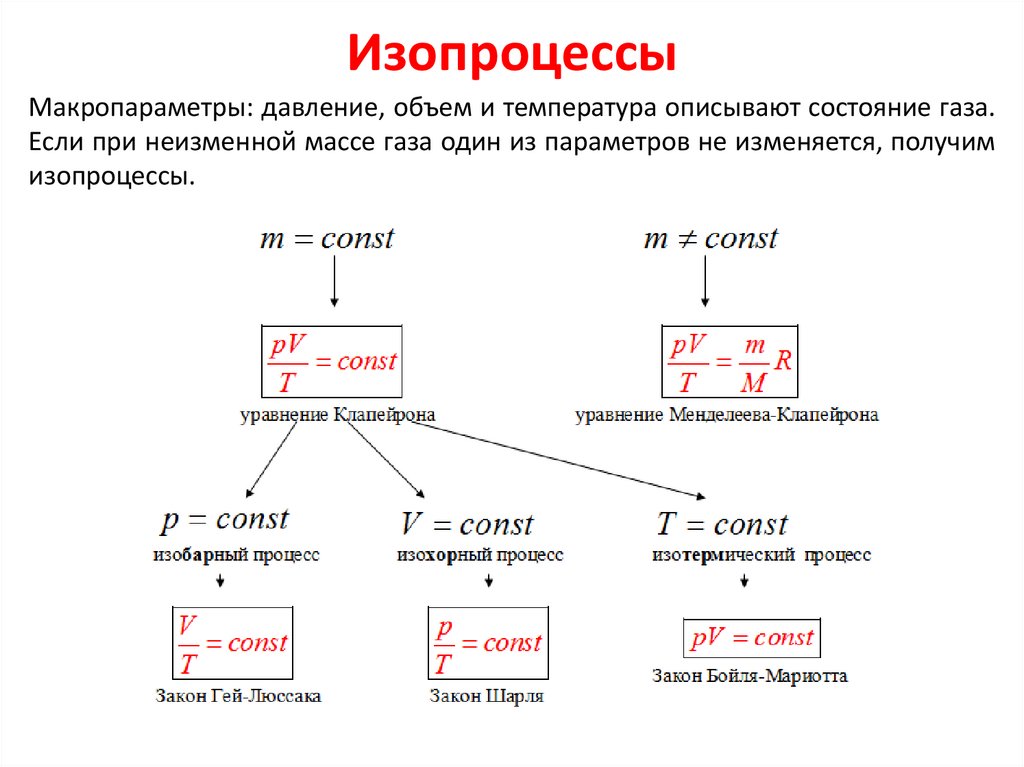
ИзопроцессыМакропараметры: давление, объем и температура описывают состояние газа.
Если при неизменной массе газа один из параметров не изменяется, получим
изопроцессы.
41.
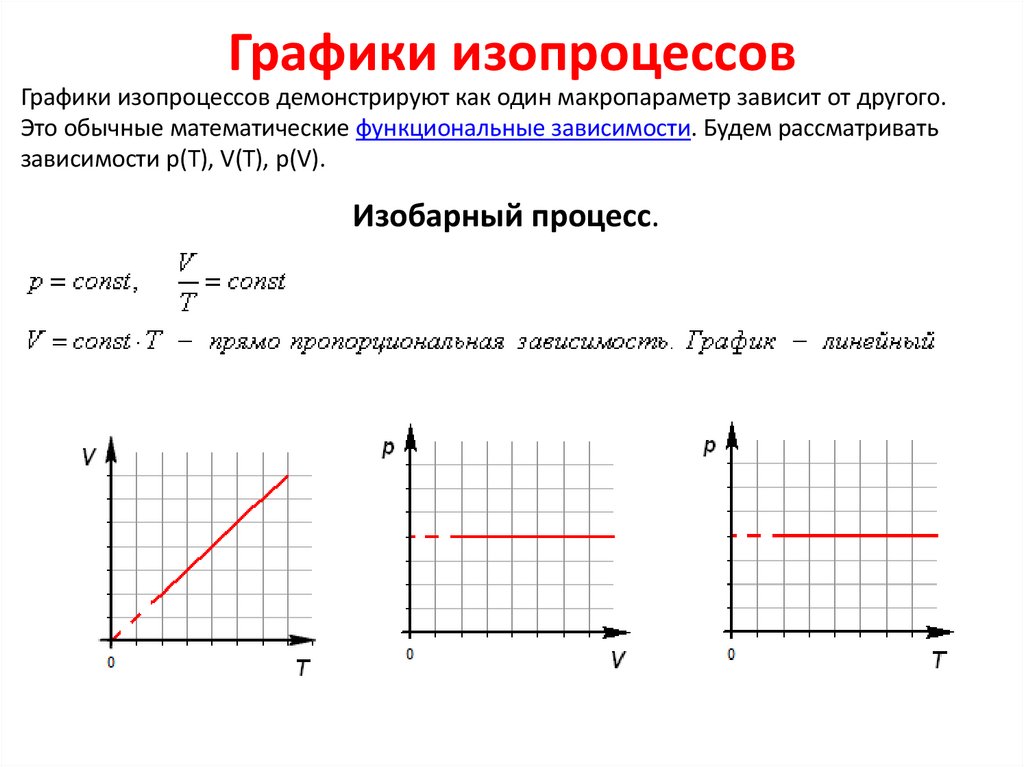
Графики изопроцессовГрафики изопроцессов демонстрируют как один макропараметр зависит от другого.
Это обычные математические функциональные зависимости. Будем рассматривать
зависимости p(T), V(T), p(V).
Изобарный процесс.
42.
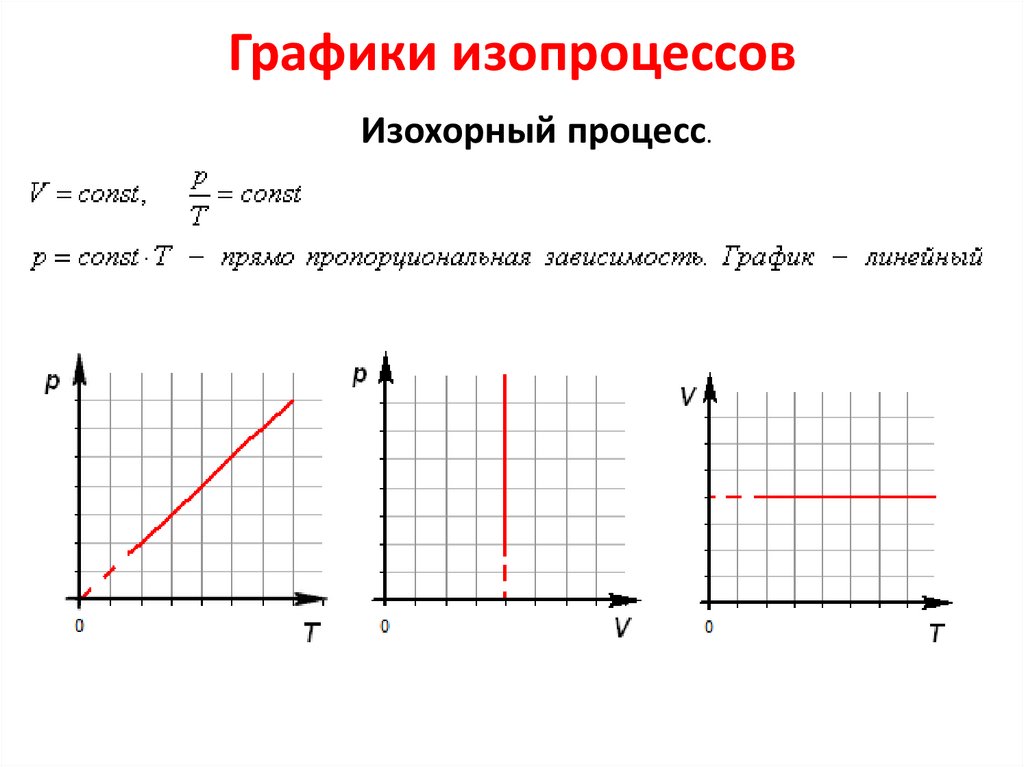
Графики изопроцессовИзохорный процесс.
43.
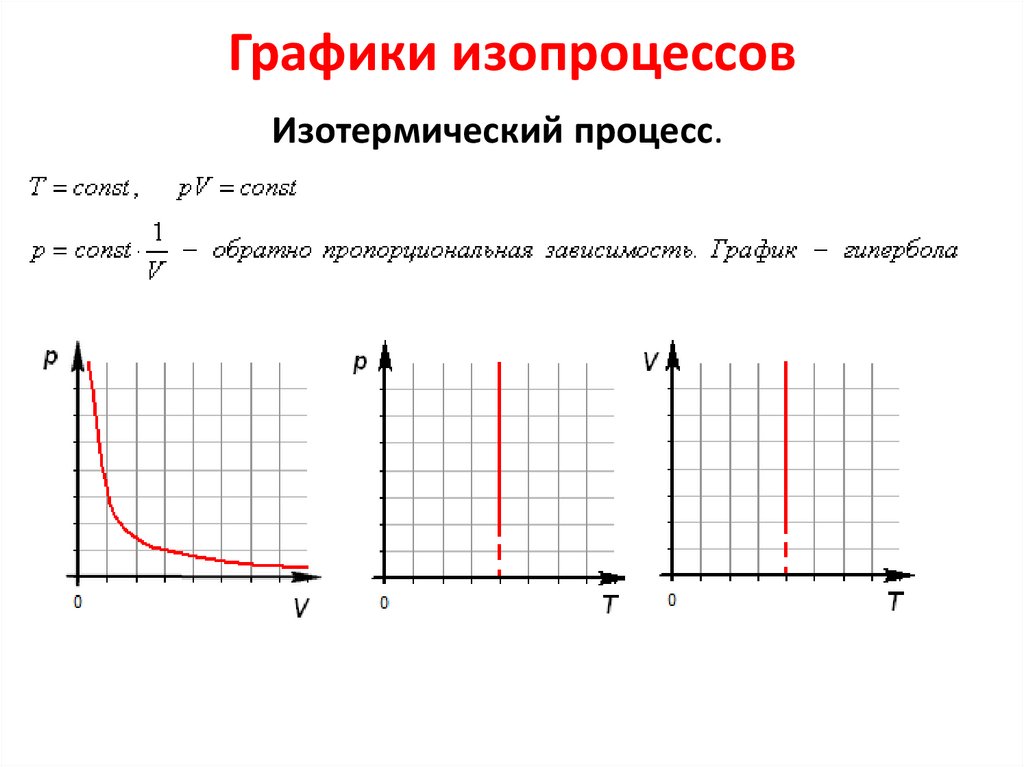
Графики изопроцессовИзотермический процесс.
44.
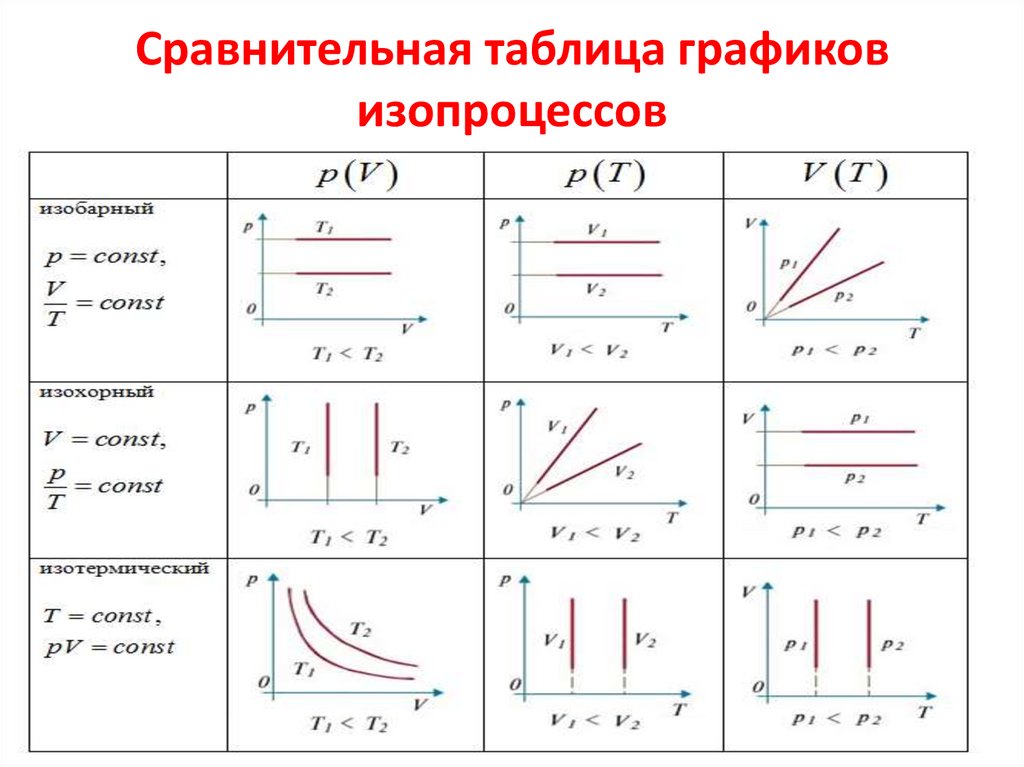
Сравнительная таблица графиковизопроцессов































 Физика
Физика








