Похожие презентации:
Электролиз
1. Цель обучения
Тема урокаЭЛЕКТРОЛИЗ
Цель обучения
10.2.3.8.- Описывать сущность процесса электролиза
2. Электролиз
Под электролизом понимают совокупность окислительно-восстановительных реакций, происходящих на электродах припрохождении постоянного электрического
тока через расплав или раствор электролита.
За
счет
электрической
энергии
при
электролизе осуществляется химическая
реакция, которая не может протекать
самопроизвольно.
3. Реакции, протекающие на электродах, называются электродными.
Электродные реакциикатодная реакция
анодная реакция
4.
Катодная реакция протекает на катоде,является реакцией восстановления
катиона:
Kt+ + e- → Kt
Анодная реакция протекает на аноде,
является реакцией окисления аниона:
An- - e- → An
5.
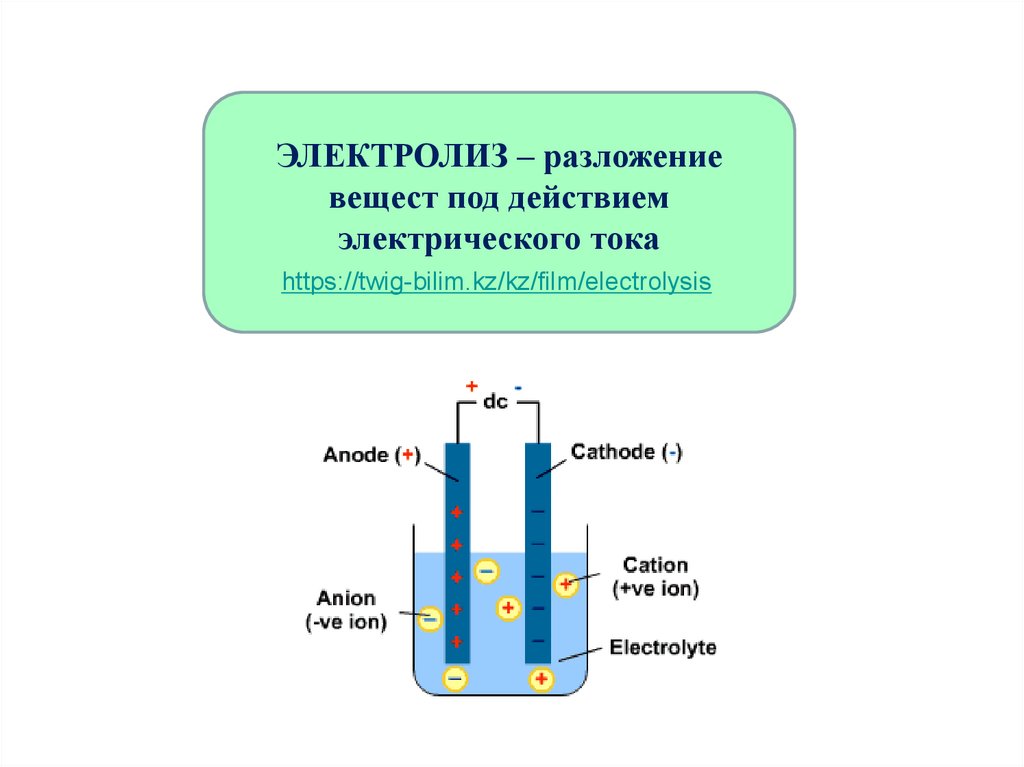
ЭЛЕКТРОЛИЗ – разложениевещест под действием
электрического тока
https://twig-bilim.kz/kz/film/electrolysis
6. Таблица. Катодные процессы в водных растворах солей
Электрохимический ряд напряжений металловLi, K, Ca,
Na, Mg, Al
Mn, Zn, Fe,
Ni, Sn, Pb
H2
Cu, Hg, Ag, Pt,
Au
Men+ +ne¯=Me0
2H2O+2e¯=H2↑+2OH¯
Men+ +ne¯=Me0
2H2O+2e¯=H2↑+2OH¯
7.
Анионы по их способности окислятьсярасполагаются в следующем порядке:
I-, Br-, S2-, Cl-, OH-, SO42-, NO3-, FВосстановительная активность анионов
уменьшается
8.
На нерастворимом (инертном) аноде впроцессе электролиза происходит окисление
анионов или молекул воды.
1. Если анион является кислотным остатком
бескислородной кислоты (например, S2-, Cl-, Br -,
J -), то на аноде окисляется анион.
2. Если анион является кислотным остатком
кислородсодержащей кислоты (например, SO42-,
NO3-, PO43-, CO32- ), то на аноде окисляется вода.
3. При окислении анионов органических кислот
происходит процесс:
2RCOO- - 2e- → R – R + 2CO2↑
9. Электролиз расплаваNaCl
+АНОД
+
КАТОД
Ионы металла
направляются к катоду,
ионы неметалла
направляются к аноду
Na+
ClNa+
-
Na+
Cl-
ClNa+
-
Cl-
10.
ЭЛЕКТРОЛИЗРАСПЛАВА БРОМИДА СВИНЦА
+ электрод
(анод)
– электрод
(катод)
Окисление
Восстановление
11.
1.2.
3.
4.
При электролизе раствора AgNO3 на катоде выделяется:
Серебро
Водород
Серебро и водород
Кислород и водород
1.
2.
3.
4.
Какой процесс происходит на инертном аноде при электролизе
раствора бромида натрия?
Окисление воды
Окисление ионов брома
Окисление меди
Восстановление меди
12.
Установите соответствие между формулойвещества и простым веществом, которое
образуется на катоде в результате электролиза
его водного раствора.
ХИМИЧЕСКАЯ ФОРМУЛА
ПРОДУКТ ЭЛЕКТРОЛИЗА
А) MgCl2
Б) AgNO3
В) CuSО4
Г) Li2S
А
1) Mg
2) H2
3) Ag
4) Li
5) S
6) Cu
Б
В
Г
13.
Установите соответствие между формулой солии продуктом, образующимся на инертном аноде
при электролизе ее водного раствора.
ФОРМУЛА СОЛИ
ПРОДУКТ НА АНОДЕ
А) Rb2SO4
Б) CH3COOK
В) BaBr2
Г) CuSО4
А
1) метан
2) сернистый газ
3) кислород
4) водород
5) бром
6) этан и углекислый газ
Б
В
Г













 Химия
Химия








