Похожие презентации:
Нитросоединения
1.
НИТРОСОЕДИНЕНИЯпроизводныеуглеводородов, в
молекулах которых один
или несколько атомов
водорода замещены на
нитрогруппу -NO2
нитро (Шевчук)
1
2.
Названиянитросоединений
образуют от названия
углеводорода, добавляя
префикс (приставку)
нитрос указанием номера атома
углерода при нитрогруппе
нитро (Шевчук)
2
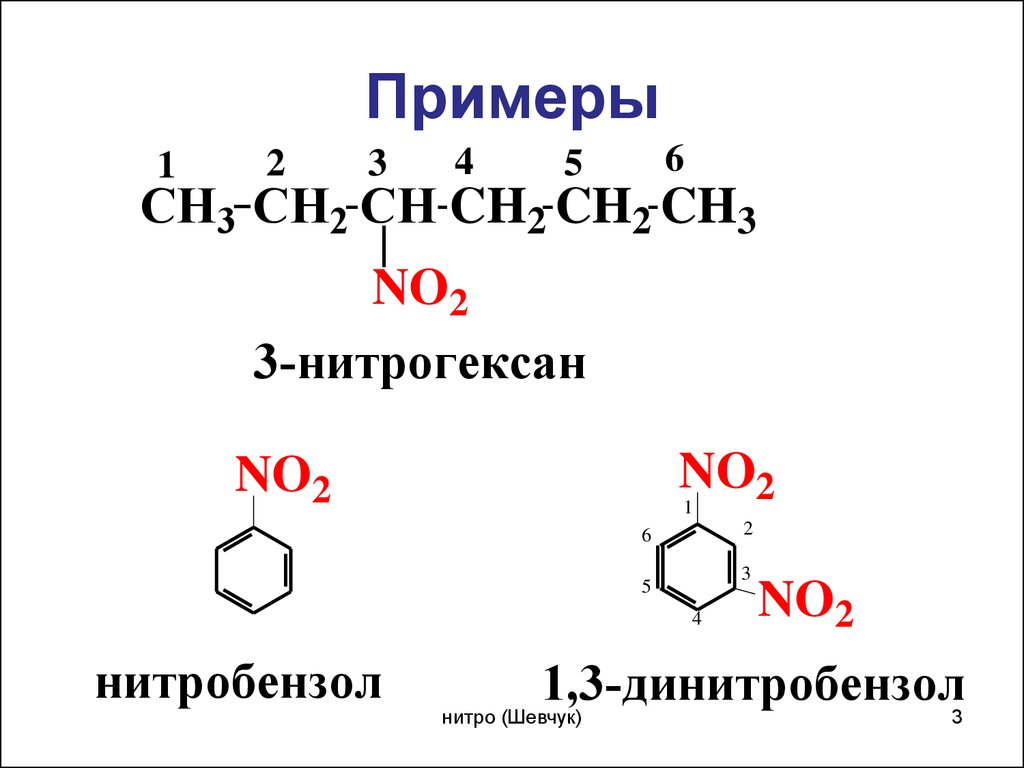
3. Примеры
12
3
4
6
5
CH3 CH2 CH CH2 CH2 CH3
NO2
3-нитрогексан
NO2
NO2
1
2
6
3
5
4
нитробензол
NO2
1,3-динитробензол
нитро (Шевчук)
3
4.
Способы получения1.
Реакции
нитрования
алканов
2. Нитрование аренов
3.Замещение галогена на
нитрогруппу
действием
нитритов (NaNO2)
(См. хим. св-ва этих классов
соединений)
нитро (Шевчук)
4
5.
ХИМИЧЕСКИЕ СВОЙСТВА1. Реакции восстановления
нитрогруппы;
2.Реакции по α-углеродному
атому;
3. Реакции по ароматическому
кольцу (реакции электрофильного замещения)
нитро (Шевчук)
5
6.
1. Восстановлениенитросоединений
а) Нитроалканы восстанавливаются
до алифатических аминов:
1) Fe, Zn, Sn в кислой среде
2) H2/Ni
3) гидридами металлов (LiAlH4)
LiAlH4
R CH2 NO2
R CH2 NH2
H2O алифатические
амины
нитро (Шевчук)
6
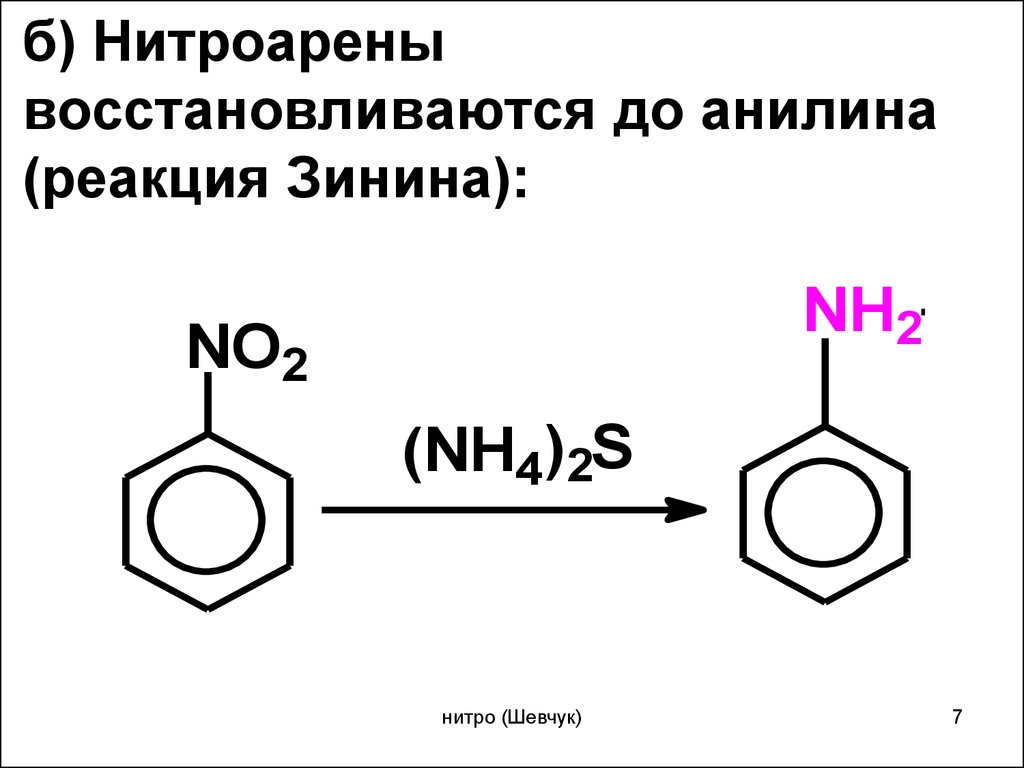
7. б) Нитроарены восстановливаются до анилина (реакция Зинина):
NH2NO2
(NH4)2S
нитро (Шевчук)
7
8.
2) реакции с азотистой кислотой(HNO2 )
Первичные и вторичные
нитроалканы можно отличить
друг от друга и от третичных
нитросоединений реакцией с
азотистой кислотой (0-5 oC)
NaNO2+HCl→HNO2 + NaCl
нитро (Шевчук)
8
9. Первичные нитросоединения с азотистой кислотой образуют продукты красного цвета Вторичные нитросоединения образуют с HNO2 синие продукты
нитро (Шевчук)9
10.
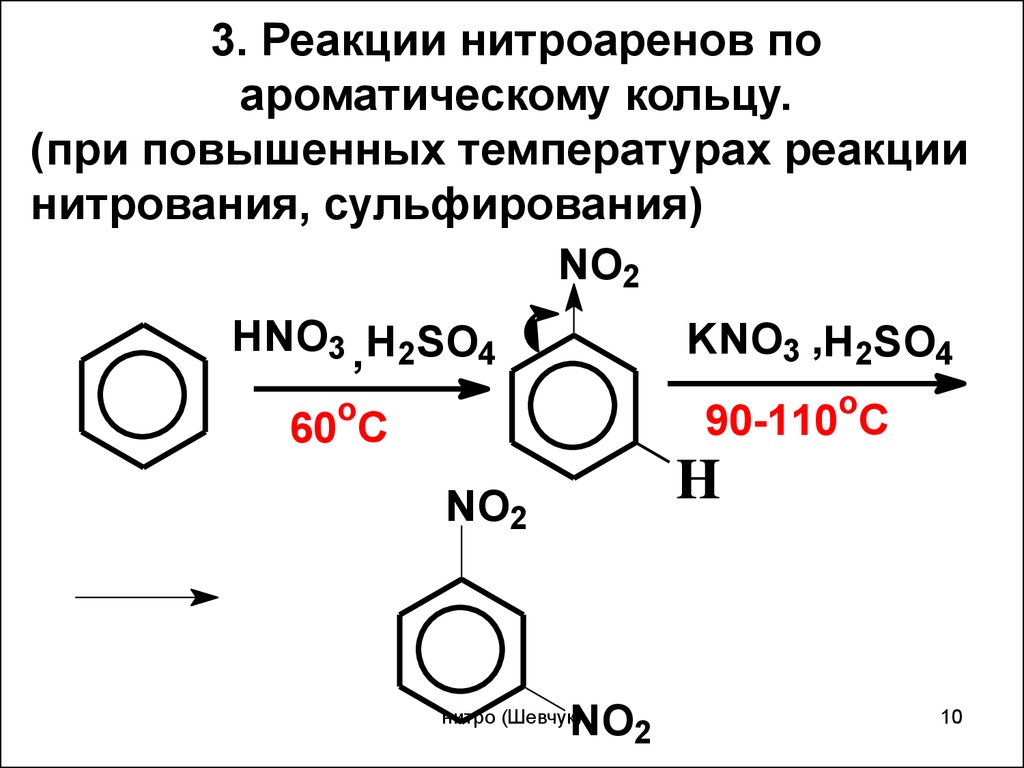
3. Реакции нитроаренов поароматическому кольцу.
(при повышенных температурах реакции
нитрования, сульфирования)
NO2
HNO3 , H2SO4
KNO3 ,H2SO4
o
o
90-110 C
60 C
H
NO2
NO2
нитро (Шевчук)
10
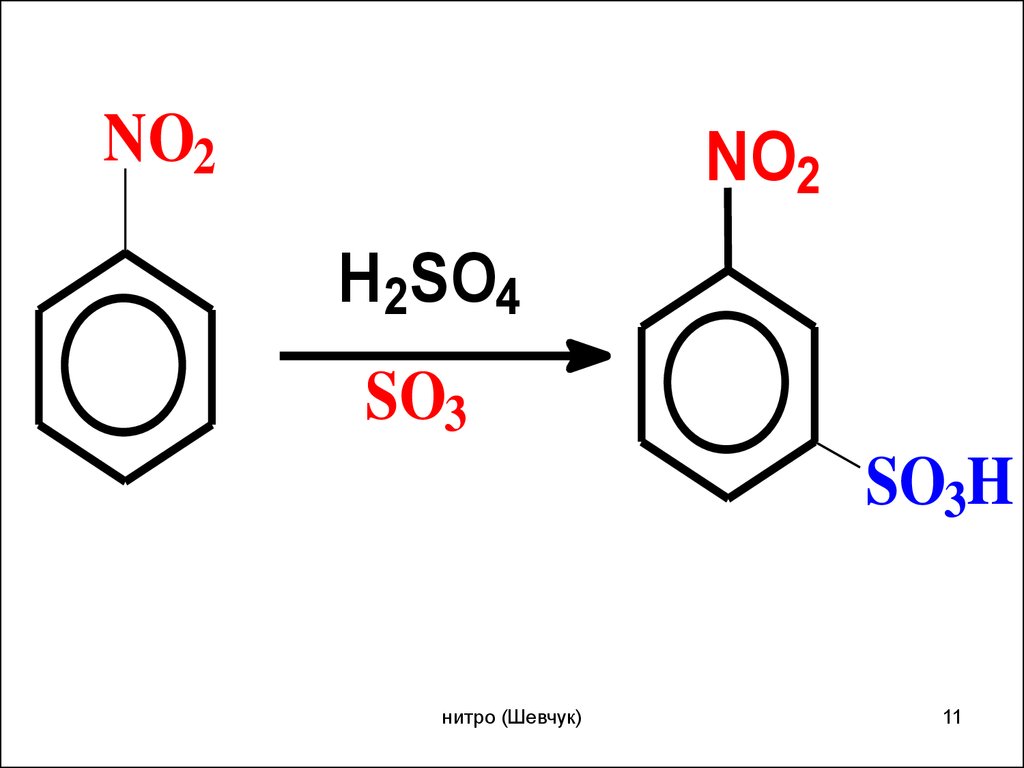
11.
NO2NO2
H2SO4
SO3
SO3H
нитро (Шевчук)
11
12. Токсичные свойства нитросоединений
Нитросоединения(особенно
ароматические) проникают в организм
через органы дыхания, пищеварения и
кожу, частично выделяются с мочой.
Симптомы острого отравления —
раздражение слизистых оболочек глаз и
дыхательных путей, возбуждение. При
тяжелых отравлениях—отек легких,
судороги, поражение печени.
нитро (Шевчук)
12
13.
Аминосоединенияпроизводные аммиака,в молекуле которого
атомы водорода
замещены
углеводородными
радикалами
нитро (Шевчук)
13
14.
В зависимости от числауглеводородных групп различают:
R NH2
первичные амины
R NH
R' вторичные амины
R N R''
третичные амины
R'
нитро (Шевчук)
14
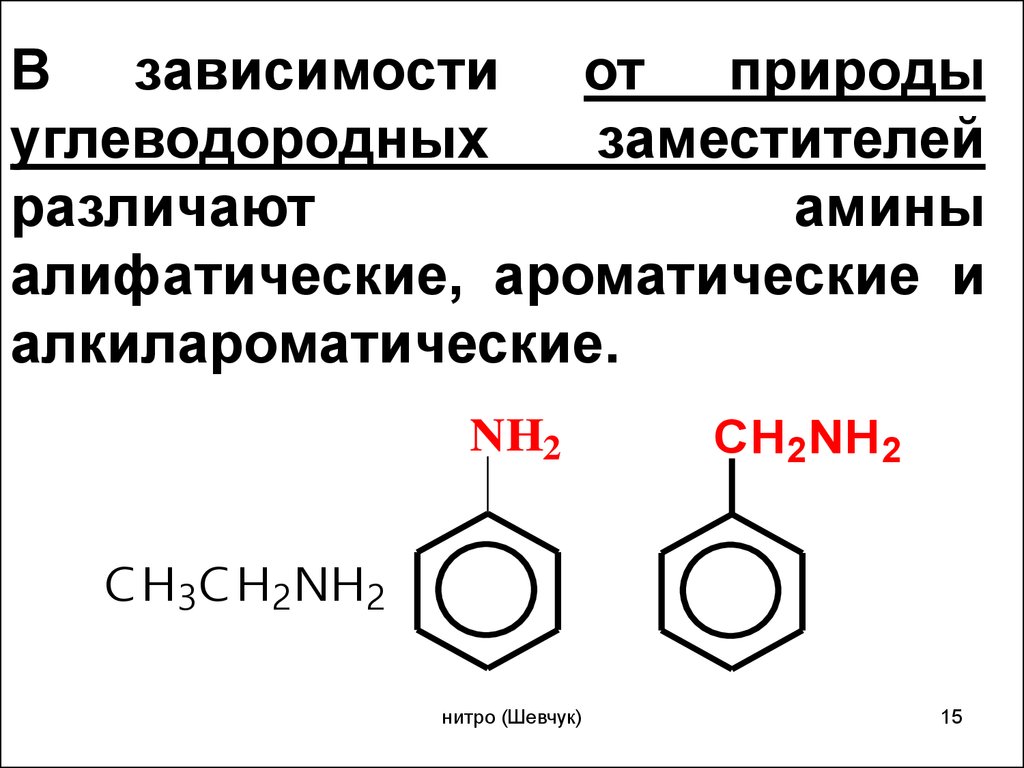
15.
В зависимости от природыуглеводородных
заместителей
различают
амины
алифатические, ароматические и
алкилароматические.
NH2
CH2NH2
C H3C H2NH2
нитро (Шевчук)
15
16.
НОМЕНКЛАТУРАЧаще всего амины называют
по рациональной
номенклатуре: к названию
углеводородных радикалов,
перечисленных от младшего к
старшему добавляют название
основы - амин
нитро (Шевчук)
16
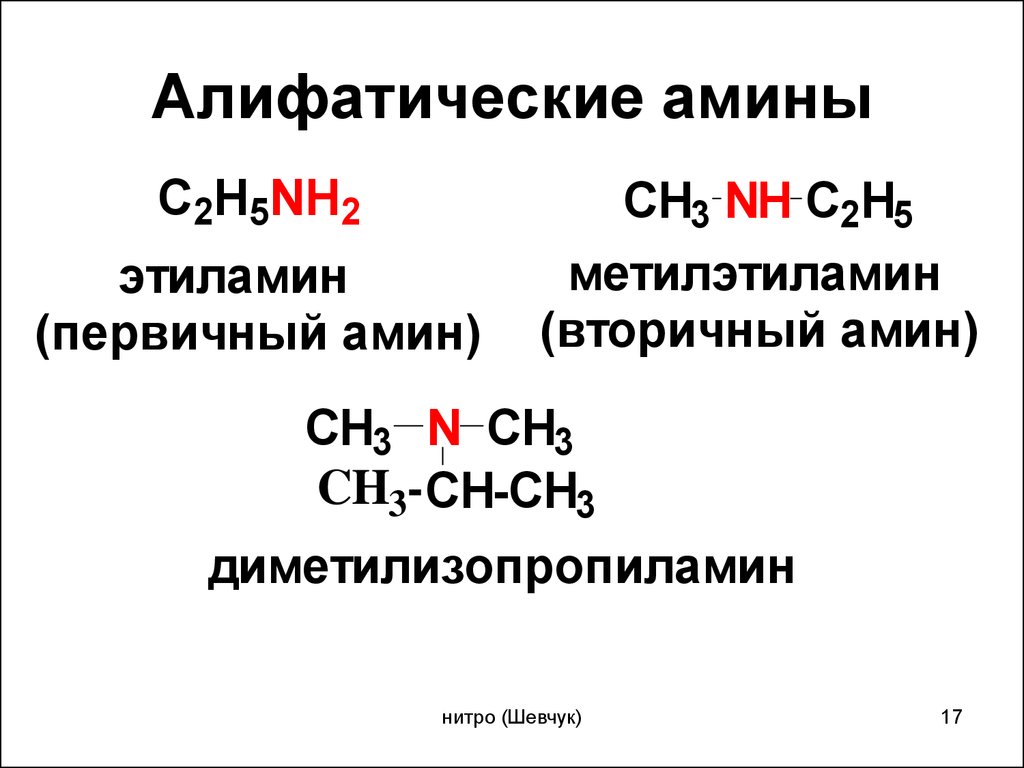
17. Алифатические амины
C2H5NH2этиламин
(первичный амин)
CH3 NH C2H5
метилэтиламин
(вторичный амин)
CH3 N CH3
CH3- CH-CH3
диметилизопропиламин
нитро (Шевчук)
17
18.
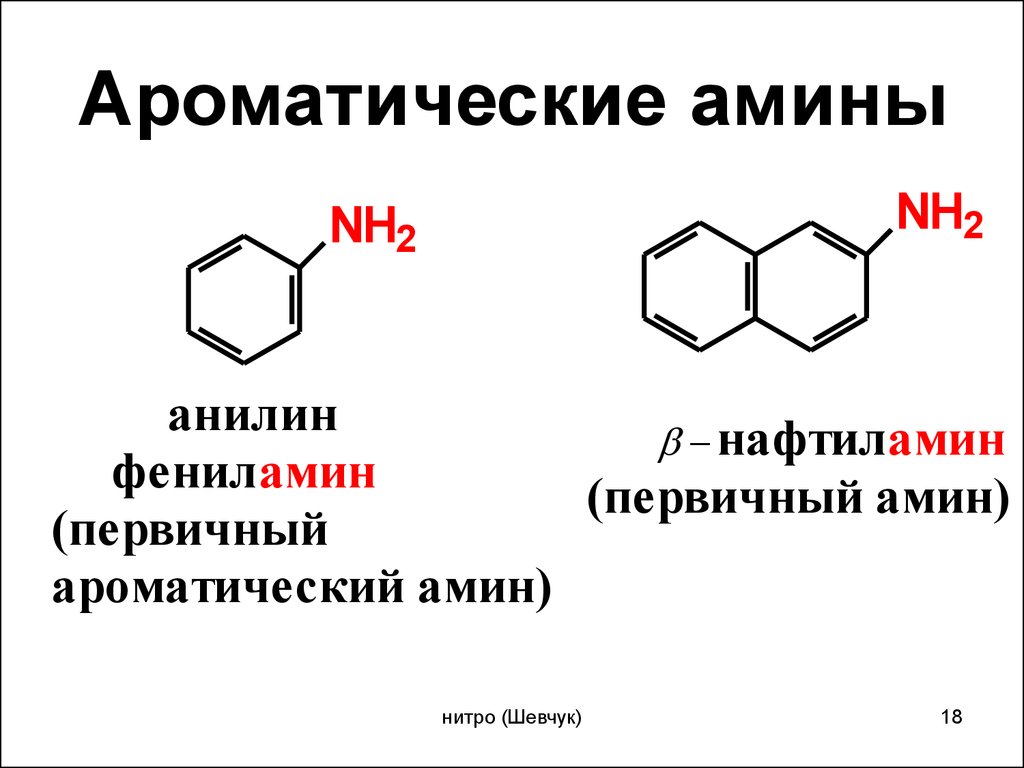
Ароматические аминыNH2
NH2
анилин
нафтиламин
фениламин
(первичный амин)
(первичный
ароматический амин)
нитро (Шевчук)
18
19.
По номенклатуре ИЮПАК названияалифатических аминов образуют от
названий
соответствующих
углеводородов (алканов) прибавлением
суффикса –амин. Номер углерода при
аминогруппе
помещают
перед
названием алкана
CH3 CH CH2CH3
NH2
2-бутанамин
нитро (Шевчук)
19
20.
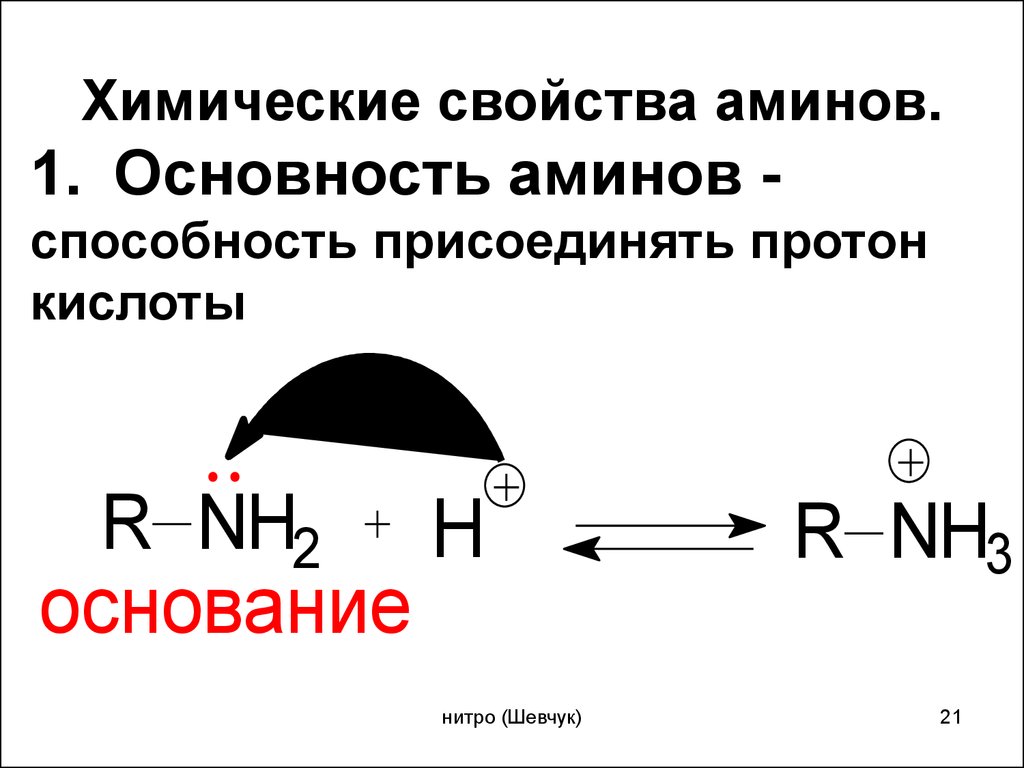
Химические свойства аминов.1. Основность аминов способность присоединять протон
кислоты
R NH2
основание
H
нитро (Шевчук)
R NH3
21
21.
2. Алкилирование аминогруппы можнопроводить галогеналканами (реакция
Гофмана) или спиртами (в
промышленности). Алкилироваться могут
первичные, вторичные и третичные
амины.
R NH2 + R1 Br
первичный
амин
OH
R NH2 R1 Br OH
соль вторичного
амина
R NH R1 + H2O+ Br
вторичный
амин
нитро (Шевчук)
22
22. 2. Алкилирование аминогруппы можно проводить галогеналканами (реакция Гофмана) или спиртами (в промышленности). Алкилироваться могут перви
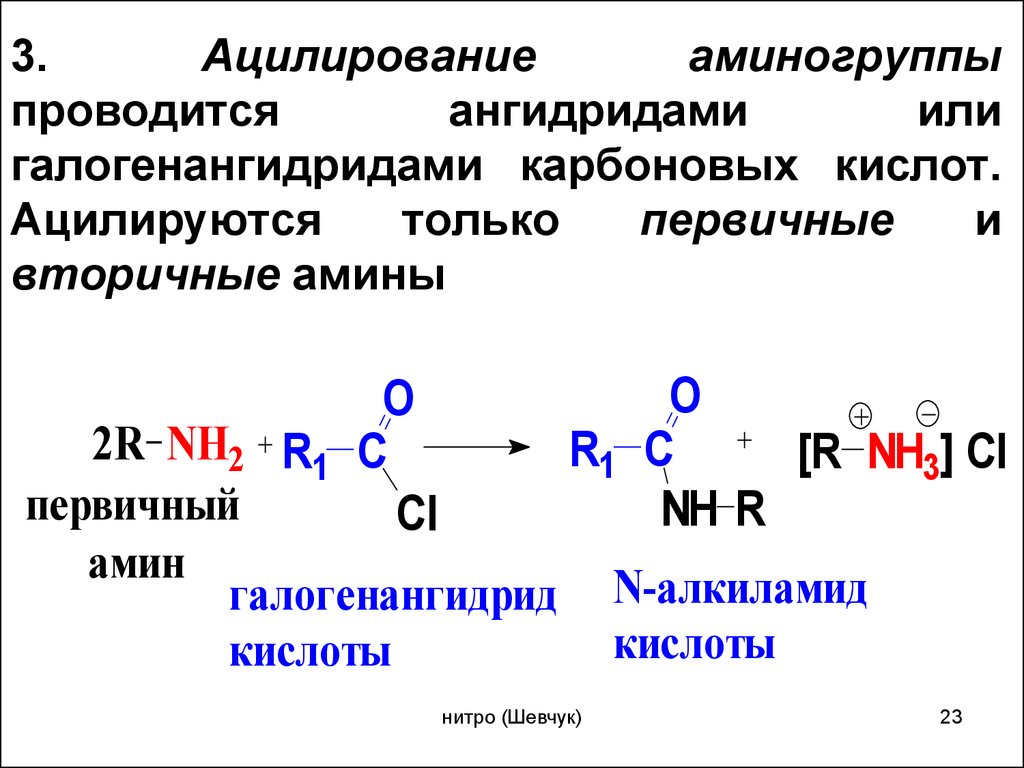
3.Ацилирование
аминогруппы
проводится
ангидридами
или
галогенангидридами карбоновых кислот.
Ацилируются
только
первичные
и
вторичные амины
O
O
2R NH2 R1 C
R1 C
[R NH3] Cl
первичный
NH R
Cl
амин
галогенангидрид N-алкиламид
кислоты
кислоты
нитро (Шевчук)
23
23. 3. Ацилирование аминогруппы проводится ангидридами или галогенангидридами карбоновых кислот. Ацилируются только первичные и вторичные ам
4. Реакции аминов с азотистойкислотой являются качественными
и позволяют различить между
собой первичные, вторичные и
третичные амины.
нитро (Шевчук)
24
24.
первичные алифатические аминыпри взаимодействии с HNO2 образуют
спирты и молекулярный азот. Реакция
сопровождается «моментальным
закипанием» реакционной смеси:
HNO2
NaNO2 + HCl
R OH + N2 + NaCl + H2O
o
0 5 C
R NH2
первичный
алифатический амин
нитро (Шевчук)
25
25.
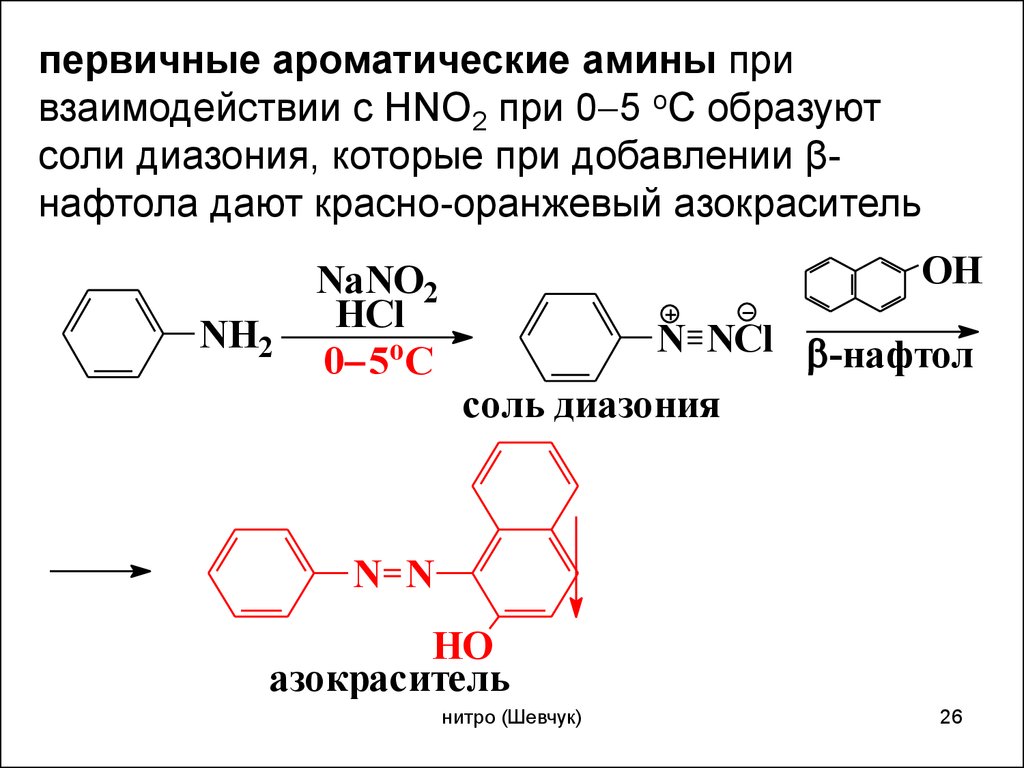
первичные ароматические амины привзаимодействии с HNO2 при 0 5 оС образуют
соли диазония, которые при добавлении βнафтола дают красно-оранжевый азокраситель
NH2
NaNO2
HCl
0 5oC
OH
N NCl -нафтол
соль диазония
N N
HO
азокраситель
нитро (Шевчук)
26
26.
вторичные амины при взаимодействии с HNO2образуют N-нитрозосоединения, которые
выпадают в виде желтых осадков или тяжелых
маслянистых жидкостей
R NH R1
NaNO2
HCl
0 5oC
R N R1 + H2O
N=O
N- нитрозодиалкиламин
нитро (Шевчук)
27
27.
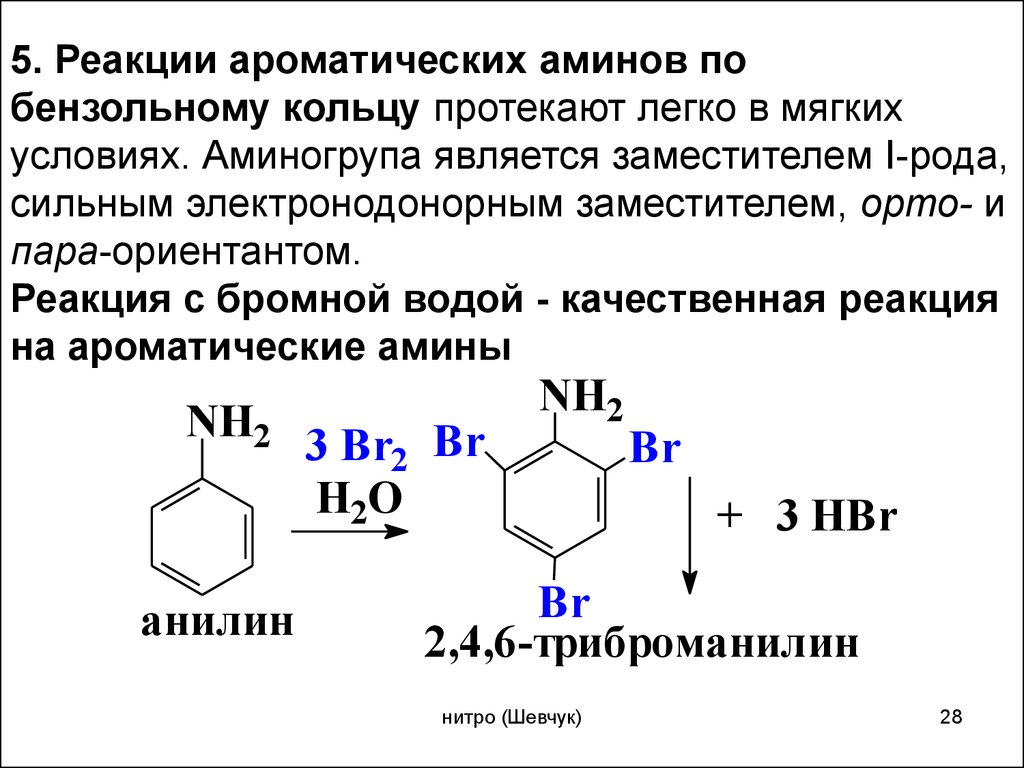
5. Реакции ароматических аминов побензольному кольцу протекают легко в мягких
условиях. Аминогрупа является заместителем I-рода,
сильным электронодонорным заместителем, орто- и
пара-ориентантом.
Реакция с бромной водой - качественная реакция
на ароматические амины
NH2
анилин
3 Br2 Br
H2O
NH2
Br
+ 3 HBr
Br
2,4,6-триброманилин
нитро (Шевчук)
28
28.
Сульфирование:NH2
H2SO4
NH3
180-200оС
HSO4
нитро (Шевчук)
NH2
SO3H
сульфаниловая
кислота
29
29.
Основные представителиаминов
Алифатические диамины – исходные
соединения
для
получения
полиамидов, например, найлона,
широко
применяемого
для
изготовления волокон, полимерных
пленок, а также узлов и деталей в
машиностроении
(полиамидные
шестерни в зубчатых передачах).
нитро (Шевчук)
30


















 Химия
Химия








